
10月27日,Intellia Therapeutics宣布该公司已暂停其在研CRISPR/Cas9体内基因编辑疗法nexiguran ziclumeran (nex-z, NTLA-2001) 针对转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)的MAGNITUDE和针对多发性神经病(ATTR-PN)的MAGNITUDE-2两项关键III期临床试验的患者给药与筛选。

此次行动源于2025年10月24日收到的一份报告:一名受试者于2025年9月30日在MAGNITUDE试验中接受nex-z给药后,出现4级肝转氨酶升高及总胆红素升高,已触发试验方案规定的暂停标准。该患者已入院,正接受密切监护和医学干预。Intellia正与专家磋商,评估潜在风险缓解措施,并与全球监管机构保持沟通。
截至发稿,公司股价已经暴跌42%。

今年5月,Intellia曾披露另一名接受nex-z治疗的患者出现了4级肝酶升高,该公司当时并未选择暂停给药。根据Intellia公司2022年8月发布的新闻稿,Nex-z在I期ATTR-PN研究中也曾出现肝酶显著升高。尽管患者肝脏信号在28天后无症状且无需医疗干预即可恢复正常,但Intellia当时修改了研究方案,并引入了较低剂量的nex-z固定治疗方案。
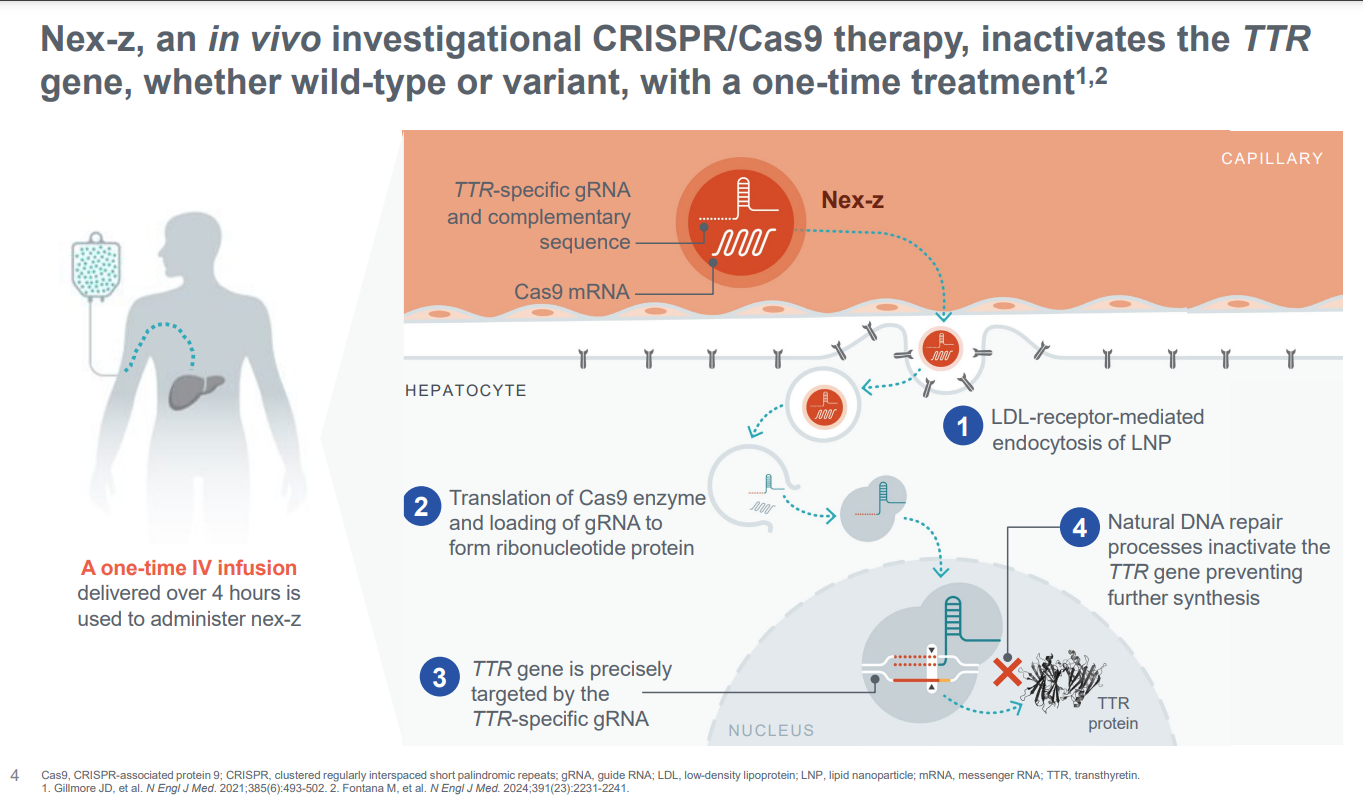
Nex-z是基于CRISPR/Cas9技术开发的体内基因编辑疗法,旨在通过单次静脉输注,利用脂质纳米颗粒 (LNP) 递送系统将基因编辑工具靶向递送至肝脏,精准敲除转甲状腺素蛋白 (TTR) 的基因,从源头阻断致病蛋白的产生。
今年5月,Intellia公布了 nex-z 治疗ATTR淀粉样变性伴多发性神经病 (ATTRv-PN)Ⅰ期临床试验两年随访数据。结果显示,nex-z能显著且持续地降低患者的TTR水平,同时患者临床症状有所改善。对于安全性,公司表示观察到的肝酶异常不被认为严重,无症状且在没有医疗干预或后遗症的情况下自发消退。
截至目前,已有超过650名ATTR-CM患者入组MAGNITUDE试验,47名ATTR-PN患者入组MAGNITUDE-2试验;其中估计超过450名患者已接受nex-z给药。
Intellia总裁兼首席执行官John Leonard医学博士表示:“基于对患者安全的承诺,我们已立即暂停MAGNITUDE和MAGNITUDE-2的入组,同时对该事件展开深入调查。在全力保障这位患者健康的同时,我们也将与监管机构及其他利益相关方合作,尽快制定合适的重启入组策略。”
参考资料:公司公告
扩展阅读:
2. 千万美元里程碑付款 礼来合作开发RNAi基因疗法新药申请获授权
3. 基因疗法加入减肥药大战
4. 2025年CGT领域融资热潮:10家CGT公司完成融资!眼科基因疗法领航,iPSC与靶向递送技术并进
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!




































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)

















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论