
11月27日,据CDE官网公示,江苏万高药业提交的盐酸曲唑酮缓释片上市申请已获受理。据摩熵医药数据库显示,该品种在国内暂无药企获批,江苏万高药业角逐首仿抢占百亿市场。
截图来源:CDE
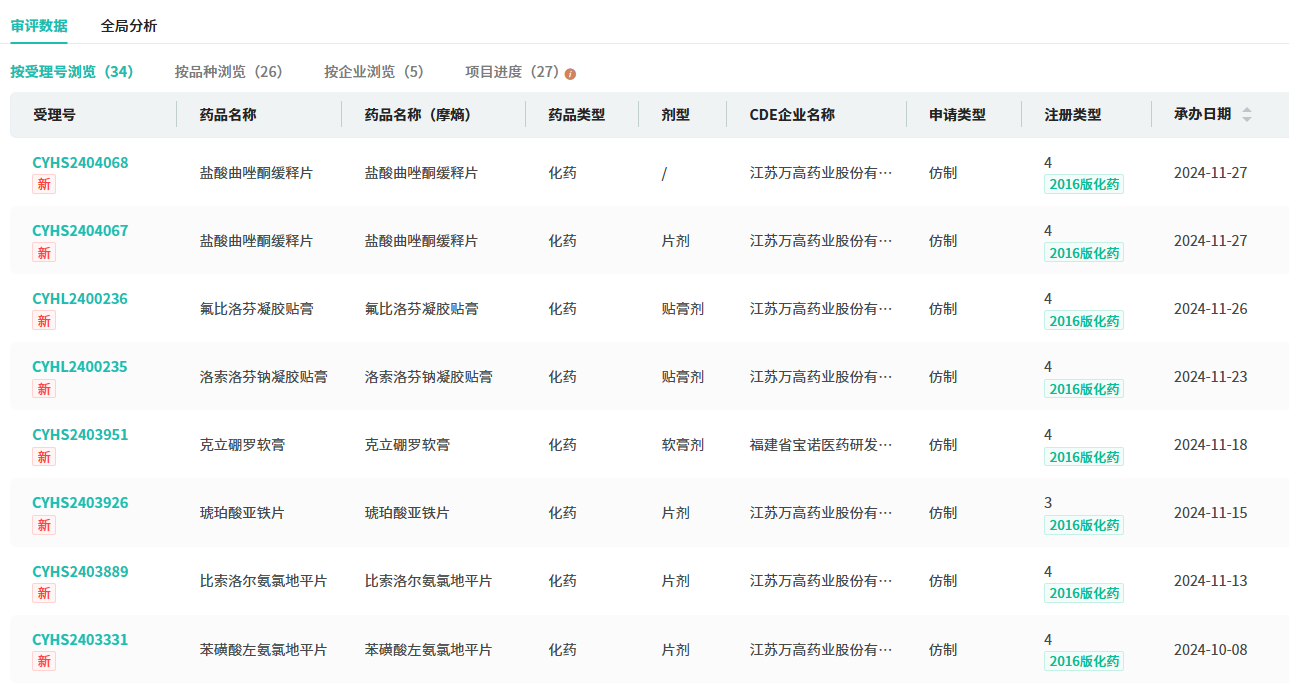
曲唑酮是20世纪60年代由Angelini Research Laboratories最先研发,作为苯基哌嗪和三唑并吡啶衍生物,在临床上被归为5-HT2拮抗剂/再摄取抑制剂(SARI)类抗抑郁药物,属于第二代抗抑郁药物。据《2022年中国抑郁症蓝皮书》显示,目前我国已有9500万抑郁症患者,抗抑郁药物市场规模已超过百亿元,且飞速增长。2020年,NMPA批准盐酸曲唑酮缓释片上市,用于治疗抑郁症。目前,盐酸曲唑酮缓释片已被纳入国家医保目录。据摩熵医药数据库显示,盐酸曲唑酮缓释片在2023年全国院内市场的销售额超380万元,同比增长达380.77%。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论