1.1.1 总体概况
根据摩熵医药数据库统计,2025.10.27-2025.11.02期间共有70个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号59个,进口药品受理号11个。
本周共计75款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药38款,生物药33款,中药4款。其中值得注意的有:
(1)MAX-001胶囊
10月27日,CDE官网公示:安炎达医药的MAX-001胶囊获得临床试验默示许可,拟用于晚期实体瘤。公开资料显示,MAX-001是一款具备全新化学骨架的新一代高选择性COX-2抑制剂,在较低剂量水平即可显著降低肿瘤微环境中的PGE2水平,进而恢复机体正常免疫功能。
(2)ADC-118片
10月28日,CDE官网公示:艾迪药业的ADC-118片获得临床试验默示许可,拟用于作为完整方案治疗人类免疫缺陷病毒1型(HIV-1)感染的成人。公开资料显示,ADC-118是一款HIV整合酶抑制剂复方制剂,是艾迪药业以其全新化学结构的HIV整合酶抑制剂Asuptegravir(ASU,项目代号:ACC017)为核心,联合恩曲他滨、丙酚替诺福韦组成的三联复方制剂(ACC017/FTC/TAF)。其可通过抑制HIV整合酶活性,有效阻断HIV基因组整合进入宿主基因组DNA。
(3)SYH-2070注射液
10月28日,CDE官网公示:石药集团的SYH-2070注射液获得临床试验默示许可,拟用于治疗高脂血症。公开资料显示,SYH-2070是一款通过偶联乙酰半乳糖胺(GalNAc)实现肝脏靶向递送的siRNA药物,以皮下给药的方式靶向血管生成素样蛋白3(ANGPTL3),能有效降低ANGPTL3水平。通过优化序列和化学修饰的策略,能实现更持久的基因沉默效果。
本周1款新药获批上市,10月30日,国家药监局发布药品批准证明文件信息:乐普生物的注射用维贝柯妥塔单抗获批上市,用于既往经至少二线系统化疗和PD-1/PD-L1抑制剂治疗失败的复发/转移性鼻咽癌患者。公开资料显示,注射用维贝柯妥塔单抗是国内首个、全球范围内临床研究进度居前的 EGFR 靶向 ADC 药物,是由抗 EGFR 人源化单抗 JMT101 与细胞毒药物甲基澳瑞他汀E(MMAE)通过可裂解的连接子 VC 偶联而成的。
1.1.2 本周获批临床创新药/改良型新药信息速览(不含补充申请)
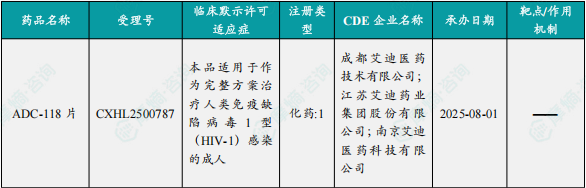
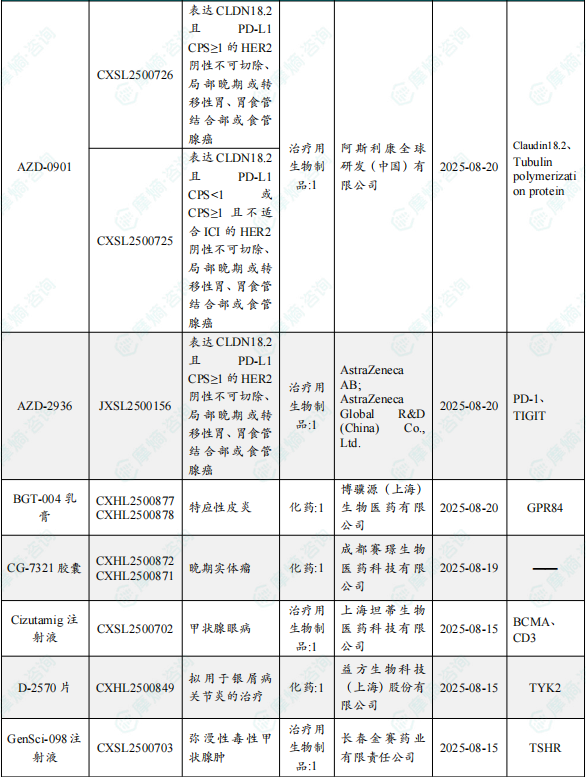
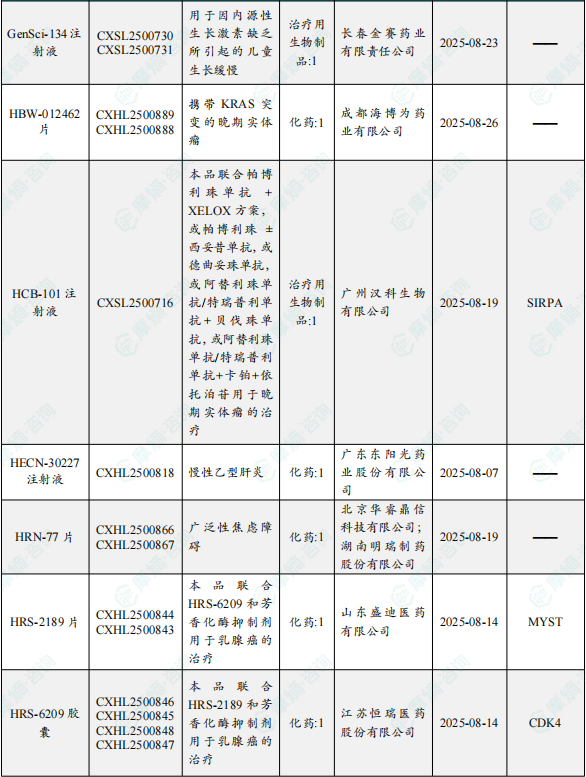
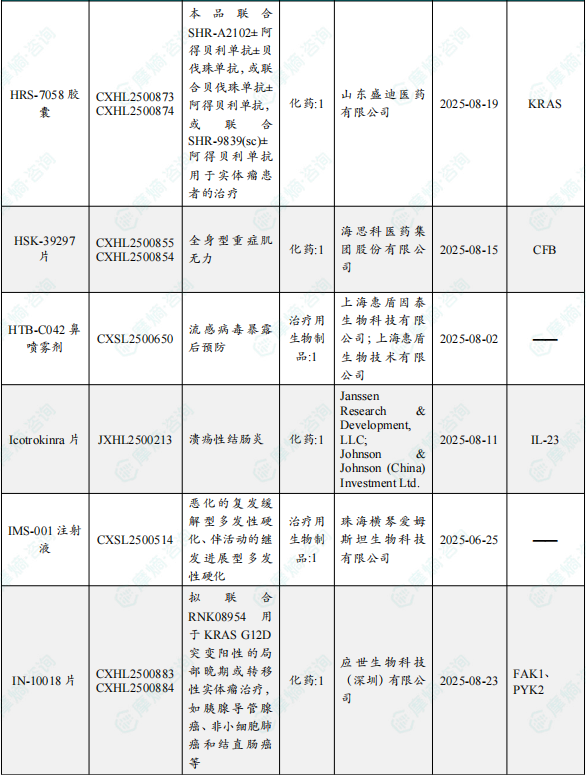
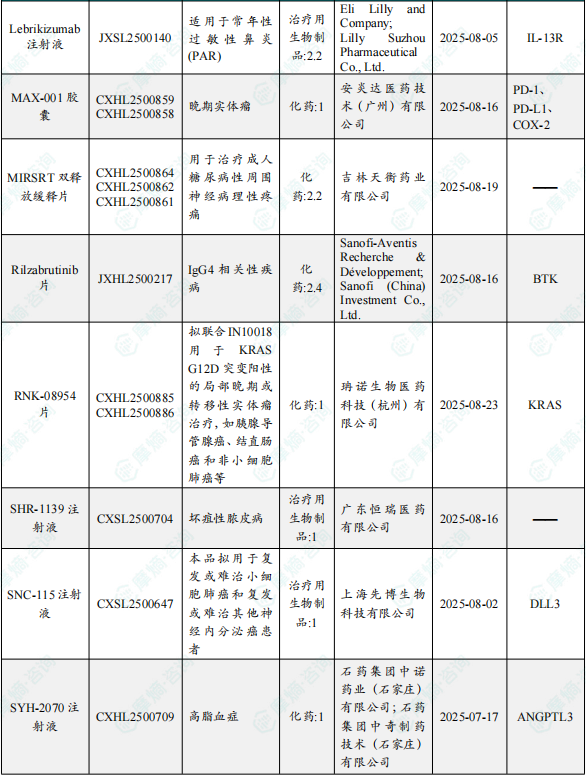
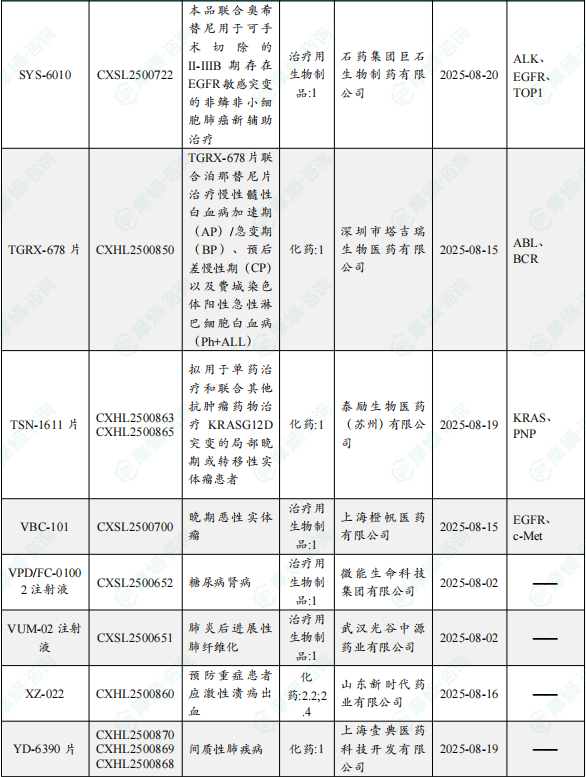
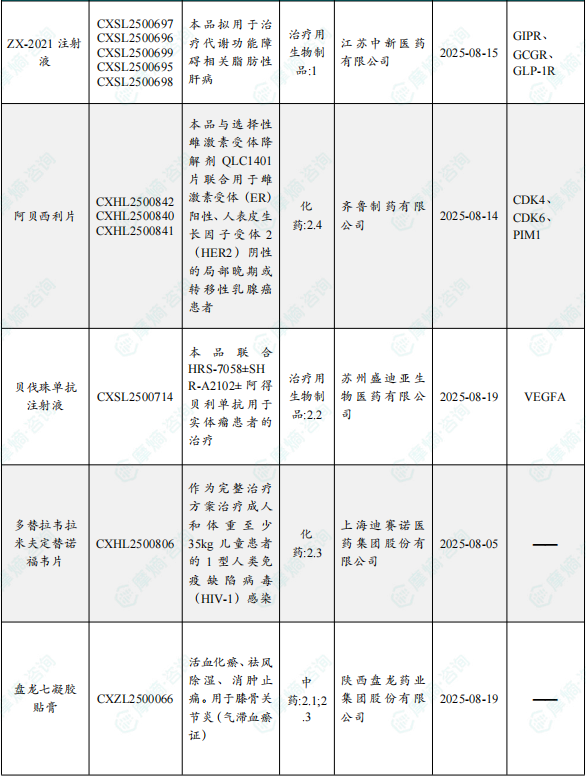
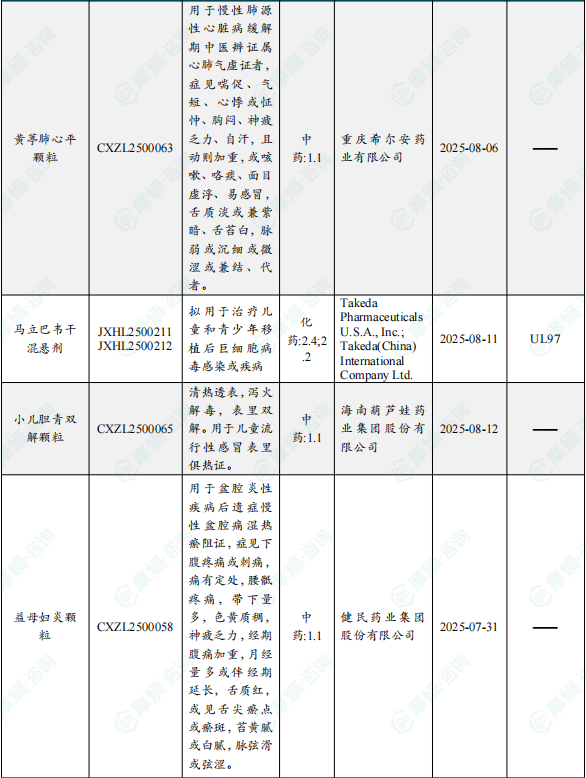
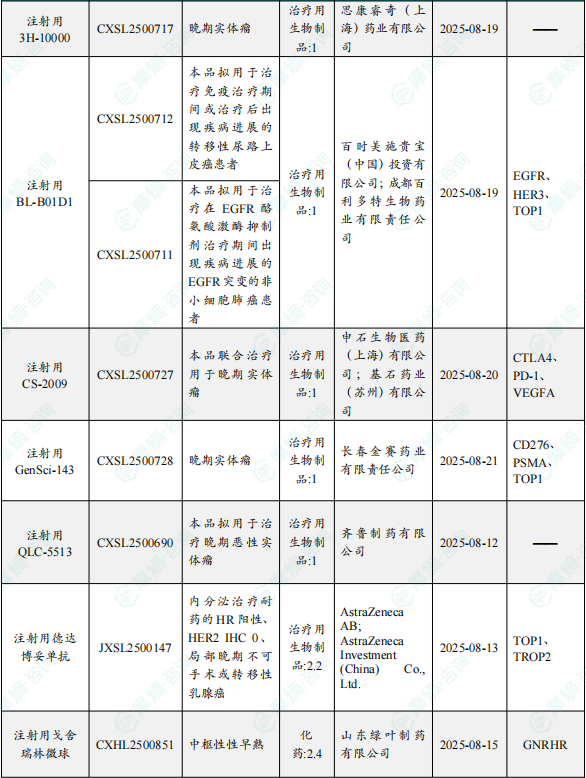
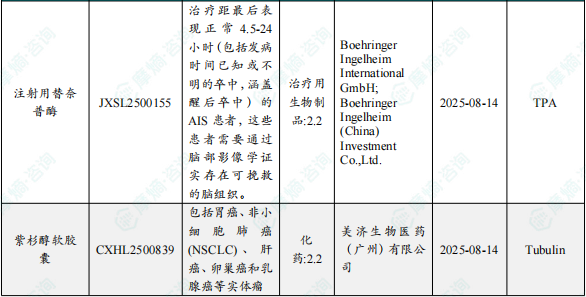
备注:(1)此处未包括补充申请之情形;(2)此处所列创新药/改良型新药,主要是指CDE受理批准的1类、2类、5.1类以及生物制品3.1类和3.2类。(3)更多获批临床信息及研发进展详情及相关靶点全局分析等,可通过摩熵中国药品审评数据库获取并下载EXCEL表格。
1.1.3 本周获批上市创新药信息速览
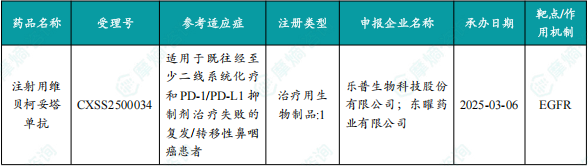
备注:(1)此处所列新药,主要是指国家药品监督管理局(NMPA)首次批准在中国上市的药品,包括新分子实体(以及包含有新分子实体的复方)、生物药、中药和疫苗。其中,新分子实体主要是化药注册分类下的1类(境内外均未上市的创新药)、5.1类(境外上市的原研药申请在国内上市);生物药主要为NMPA首次批准的国产及进口生物药;不包括生物类似物、新适应症、新剂型。(2)更多信息如获批临床品种相关靶点、研发企业、全球上市及研发进展及相关靶点全局分析等,可通过摩熵医药数据库获取并下载EXCEL表格。
同期事件:
1. 2025年第44周10.27-11.02国内仿制药/生物类似物申报/审批数据分析
2. 2025年第44周10.27-11.02国内医药大健康行业政策法规汇总
3. 2025年第44周10.27-11.02全球创新药研发概览
以上内容均来自{ 摩熵咨询医药行业观察周报(2025.10.27-2025.11.02) },如需查看或下载完整版报告,可点击!
扩展阅读:
1. 2024年第41周10.07-10.13国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2024年第42周10.14-10.20国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
3. 2024年第43周10.21-10.27国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论