
在现代药物研发的浩瀚星空中,动物模型不仅是验证药效的“试金石”,更是人类窥探生命奥秘的“活体显微镜”。回顾过去一个世纪,我们从依赖自然界随机突变的被动选择,跨越到能够精确编辑生命代码的主动创造。
这一过程不仅是生物技术的胜利,更是药物发现逻辑的根本性重塑。我将基于药物研发的历史脉络,深度剖析Wistar大鼠、免疫缺陷小鼠、转基因模型及基因敲除技术这四大里程碑,探讨它们如何一步步解除了自然进化的限制,为人类抗击疾病提供了最强有力的武器。
1. Wistar大鼠的诞生
在20世纪的钟声敲响之前,生物医学实验室更像是一个充满不确定性的“手工作坊”。那时的科学家在进行药物测试时,面临着一个巨大的变量困境——实验动物的非标准化。
1.1 从“家鼠”到“科研仪器”的跨越
直到1906年以前,实验室里使用的主要还是随处可见的普通家鼠(Mus musculus)。这些老鼠遗传背景杂乱,个体差异极大,导致实验数据的可重复性极差。药物研发人员往往陷入一种窘境:药物的无效究竟是因为分子结构的问题,还是因为这只老鼠本身体质特殊?
这一困局在1906年被打破。位于费城的Wistar研究所,在米尔顿·格林曼(Milton Greenman)和亨利·唐纳森(Henry Donaldson)的主导下,引入了一种属于褐家鼠(Rattus norvegicus)的白化大鼠品种——Wistar大鼠。这一历史性时刻标志着科研人员开始有意识地将“纯种”概念引入动物模型。
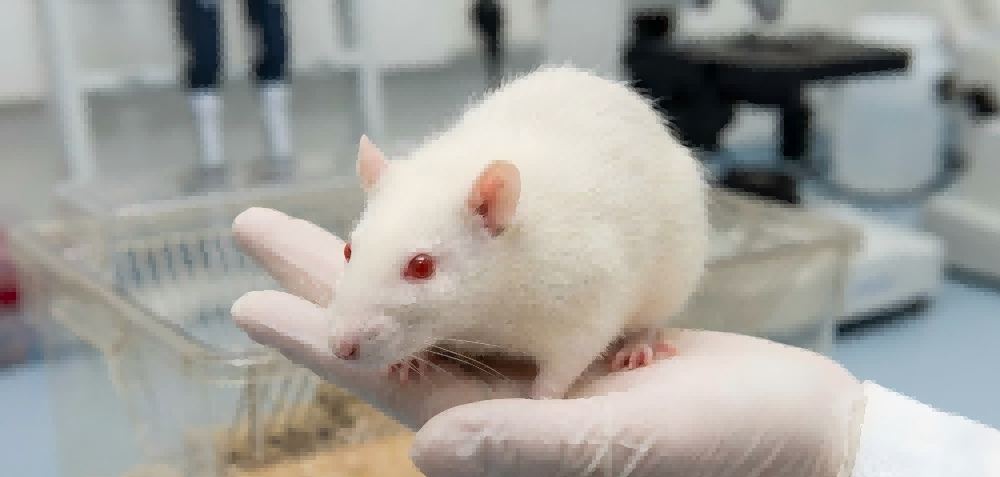
Wistar大鼠不仅仅是一种动物,它更像是一个被精密校准的“生物仪器”。据统计,当今全球实验室中超过50%的大鼠品系都流淌着Wistar研究所原始鼠种的血液。它的出现,让药物研发第一次拥有了相对稳定的“生物基准线”。
1.2 自然突变的宝库
Wistar大鼠的价值不仅在于其标准化的遗传背景,更在于其庞大的亚种群分化。在那个无法进行基因编辑的年代,科学家们通过敏锐的观察和选择性育种,从Wistar大鼠的后代中筛选出了多种具有特定病理特征的模型。这些模型成为了当时研究人类复杂疾病的唯一窗口:
- 代谢性疾病的突破:科学家们培育出了自发性糖尿病大鼠,让胰岛素及降糖药的研发有了活体验证平台。
- 心血管与神经科学的基石:在高血压研究领域,自发性高血压大鼠成为了应用最广泛的模型;而Wistar京都大鼠则成为了研究注意力缺陷障碍(ADHD)的重要工具。
- 肿瘤与免疫:从自发肿瘤成型的Rochester品系到前列腺癌模型(Lobund-Wistar),这些自然突变的积累为早期的抗癌药物筛选提供了宝贵资源。
Wistar大鼠的成功证明了一个核心逻辑:通过控制遗传背景,我们可以将复杂的生命体转化为可控的实验变量。 这一思想为后续百年的动物模型发展奠定了认识论基础。
2. 活体培养皿的革命
如果说Wistar大鼠解决了“一致性”的问题,那么免疫缺陷动物的出现则解决了“兼容性”的难题。在很长一段时间里,癌症研究面临着一道难以逾越的屏障——异种移植排斥。人类的肿瘤细胞一旦植入动物体内,就会被动物的免疫系统无情绞杀,导致科学家无法在活体环境中研究人类癌症。
2.1 裸鼠
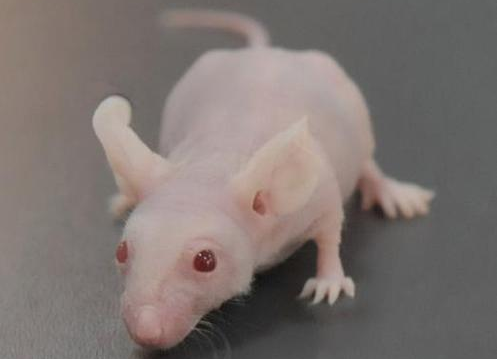
1962年,英国格拉斯哥鲁奇尔医院的病毒实验室里,一只奇怪的小鼠引起了研究人员的注意。它全身无毛,且先天性缺失胸腺。这一自然突变(Foxn1基因突变)导致它无法产生成熟的T淋巴细胞。
在当时看来,这只小鼠是病态的;但在药物研发者眼中,这是完美的“受体”。由于缺乏细胞免疫功能,裸鼠无法对外来组织产生排斥反应。这意味着,人类的肿瘤组织、器官甚至原本无法在动物体内生存的细胞,都可以像在培养皿中一样在裸鼠体内生长。
裸鼠迅速成为了肿瘤学研究的“金标准”。科学家们第一次能够观察人类肿瘤在活体内的血管生成、转移过程以及对化疗药物的反应。它实际上成为了一个长着腿的、有血液循环的“人体肿瘤培养箱”。
2.2 SCID小鼠
科学的探索永无止境。虽然裸鼠缺乏T细胞,但它仍保留了B淋巴细胞和其他免疫成分。1983年,福克斯蔡斯癌症中心(Fox Chase Cancer Center)发现了更为彻底的免疫缺陷模型——重症联合免疫缺陷(SCID)小鼠。
SCID小鼠体内发生了一种常染色体隐性突变,导致T淋巴细胞和B淋巴细胞双重缺失。这种小鼠对病原体高度易感,其身体环境对异种移植物的“宽容度”达到了前所未有的高度。
SCID小鼠的出现,不仅进一步推动了肿瘤异种移植的研究,更为传染病学打开了新大门。许多专一感染人类的病毒,在拥有完整免疫系统的动物体内无法存活,而在SCID小鼠体内则能模拟出感染进程。这为艾滋病、肝炎等病毒性疾病的药物筛选提供了不可替代的平台。
3. 转基因技术的降临
直到20世纪70年代中期,人类对动物模型的改进主要还停留在“发现”和“筛选”阶段,即依赖大自然偶然抛出的突变骰子。然而,随着分子生物学的爆发,科学家们开始不满足于等待,他们渴望主动“编写”生命。
3.1 跨越物种的基因转移
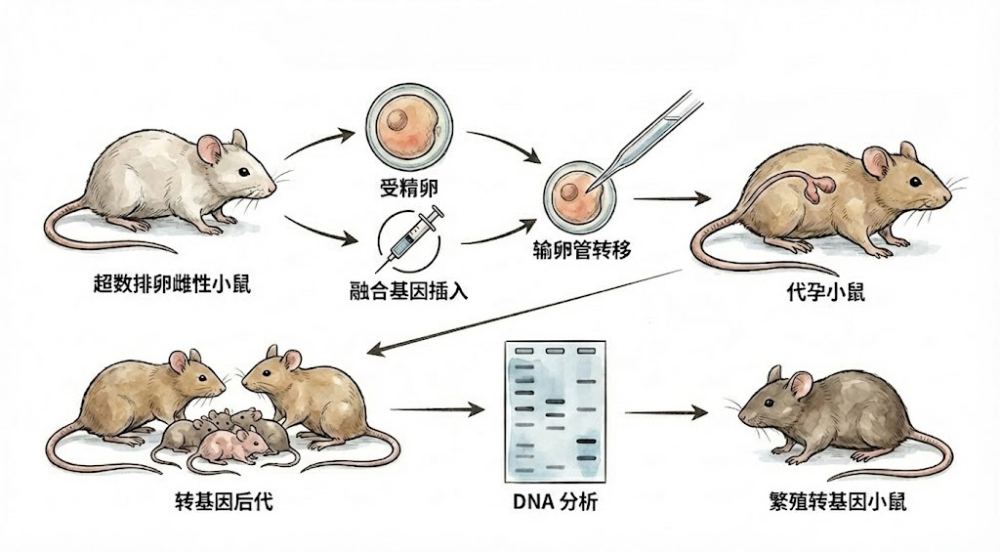
1974年,鲁道夫·贾尼施(Rudolf Jaenisch)完成了一项惊世骇俗的实验,他成功将猿猴病毒40(SV40)的DNA序列插入到了小鼠的基因组中。虽然这次尝试中的外源基因未能遗传给后代,但它推开了转基因动物时代的大门——人类首次证明,外源DNA可以被整合进哺乳动物的体内。
随后的几年里,耶鲁大学和牛津大学的研究团队完善了这项技术,通过显微注射将外源DNA注入受精卵,成功实现了基因的生殖系传递。这意味着,我们人为添加的基因,可以像原本的基因一样,一代代传下去。
3.2 为疾病“定制”模型
转基因技术的出现,彻底改变了药物研发的逻辑。我们不再需要漫无目的地寻找患有某种疾病的动物,而是可以直接将导致人类疾病的致病基因“安装”到动物体内。
- 阿尔茨海默病(AD):这种只在人类中高发的老年病,自然界中几乎找不到合适的动物模型。通过转基因技术,科学家将诱导产生β-淀粉样蛋白(Aβ42)的人类DNA转入小鼠,制造出了具有典型AD病理特征(如脑内斑块)的小鼠模型。这让AD药物的研发从“无的放矢”变成了“有的放矢”。
- 病毒感染机制:许多病毒(如HIV、脊髓灰质炎病毒)只感染人类,因为动物细胞表面缺乏特定的受体。通过转基因技术,让小鼠表达人类的病毒受体蛋白,小鼠就能被感染,从而用于疫苗和抗病毒药物的测试。
3.3 动物作为“生物制药工厂”
转基因技术的另一大应用是“生物反应器”。通过基因工程,我们可以让动物(如山羊、奶牛或小鼠)在乳汁或血液中表达具有高价值的药用蛋白。书中提到的人源抗凝血酶、纤维蛋白原以及各种单克隆抗体,都可以通过转基因动物进行大规模生产。这不仅是模型的革命,更是制药工业生产方式的革命。
4. 基因敲除与反向工程
如果说转基因技术是给生命这部书“加页”,那么基因敲除技术就是精准地“撕页”。在20世纪80年代末,随着对基因功能研究的深入,科学家们面临一个终极问题:要知道一个基因究竟有什么用,最好的办法就是把它拿掉,看生物体会出什么毛病。
4.1 胚胎干细胞与同源重组的魔法
1989年,马里奥·卡佩奇(Mario Capecchi)、马丁·埃文斯(Martin Evans)和奥利弗·史密斯(Oliver Smithies)不仅在理论上,更在实践中攻克了这一难题。他们利用小鼠胚胎干细胞(ES cells)和同源重组技术,实现了对特定基因的精准剔除。这项工作是如此具有开创性,以至于三位科学家在2007年共同分享了诺贝尔生理学或医学奖。

基因敲除的核心原理在于利用一段人工合成的、与目标基因序列相似但含有失活突变的DNA片段(靶向载体),去“诱骗”细胞自身的修复机制,将染色体上正常的基因“置换”下来。
4.2 基因敲除模型的实战价值
基因敲除小鼠的出现,让人类第一次拥有了大规模解析基因功能的工具,也为药物研发提供了极其精准的病理模型:
- 癌症机制的解密(p53):p53基因被称为“基因组的守护者”。通过敲除p53基因,科学家培育出了极易患癌的小鼠,这完美模拟了人类的李-佛美尼综合征(Li-Fraumeni syndrome)。这种模型成为测试抗癌药物防癌、治癌效果的顶级平台。
- 心血管疾病的模拟(ApoE):载脂蛋白E(ApoE)基因敲除小鼠表现出严重的高胆固醇血症,并会自发形成血管斑块。这与人类动脉粥样硬化的病理过程惊人相似,是降脂药物和抗动脉硬化药物研发的必经之路。
- 神经与代谢疾病:Fmr1基因敲除用于研究脆性X综合征(智力低下);Nhlh2基因敲除则揭示了肥胖的神经内分泌机制。
从数千种基因敲除小鼠的建立中,我们不仅确认了许多药物靶点的功能,更重要的是,我们能够预测阻断某个基因或蛋白(药物的作用机理通常如此)可能带来的副作用。
5. 结语
回顾这一百多年的历程,我们可以清晰地看到一条从“被动适应”走向“主动掌控”的清晰脉络。
① 标准化阶段(Wistar大鼠):解决了实验对象的可重复性问题,让生物学实验具备了物理学般的严谨度。
② 免疫缺陷阶段(裸鼠/SCID):解决了物种间的排斥性问题,让动物体内研究人类疾病(特别是癌症)成为可能。
③ 转基因阶段:实现了功能的获得,让我们能建立特定的人类疾病模型或生产药物。
④ 基因敲除阶段:实现了功能的缺失,让我们能通过反向工程解析基因的生物学本质。
这些里程碑式的动物模型,构成了现代药物研发大厦的基石。它们缩短了药物从实验室到病床的距离,排除了无数潜在的毒副作用,更重要的是,它们帮助我们从分子层面理解了疾病的本质。
然而,在这个技术飞速发展的时代,我们必须认识到,没有任何一种模型是完美的。转基因小鼠虽然强大,但它终究不是人。物种间的差异始终是药物研发中最大的“黑箱”。未来的方向,或许在于更人源化的动物模型,甚至是结合了类器官与AI模拟的综合系统。但无论技术如何迭代,这百年来科学家们“培育更好的模型”的初心与智慧,将永远是照亮新药发现之路的灯塔。
往期精彩:
1. 新药研发全景图:从分子发现到临床确证,再到上市后监测的挑战
2. 从长效DPP-4抑制剂奥格列汀看2型糖尿病药物:研发、市场与患者依从性的多面剖析
3. 博纳吐单抗的设计与开发:BiTE技术先锋,作用机制揭秘、临床应用挑战及与CAR-T的较量
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论