
近日,全球临床试验收录网站ClinicalTrials显示,安进公司已正式启动其创新药物AMG 133的两项关键性III期临床试验——MARITIME-1与MARITIME-2,标志着AMG 133迈入III期开发的重要阶段。


MARITIME-1是一项涉及3501名参与者的随机、双盲、安慰剂对照研究,专注于评估AMG 133(低、中、高剂量)在不伴有2型糖尿病的肥胖或超重成人中的疗效、安全性及耐受性。该试验的核心评估指标为第72周时患者体重相对于基线的百分比变化。

截图来源:摩熵医药数据库(全球药物研发数据库)
与此同时,MARITIME-2则是一项针对999名伴有2型糖尿病的肥胖或超重成人的随机、双盲、安慰剂对照试验,同样旨在探索AMG 133(低、中、高剂量)的有效性、安全性及耐受性,其关键评估指标与MARITIME-1一致。
AMG 133作为安进自主研发的突破性first-in-class抗体多肽偶联药物,通过结合全人源单抗(靶向葡萄糖依赖性促胰岛素释放多肽受体GIPR)与两个GLP-1类似物,实现了每4周一次的注射频率。该药物通过双重机制——抑制GIPR并激活GLP-1受体(GLP-1R),有效减少食物摄入、调节代谢,从而达到减轻体重和降低血糖的效果。
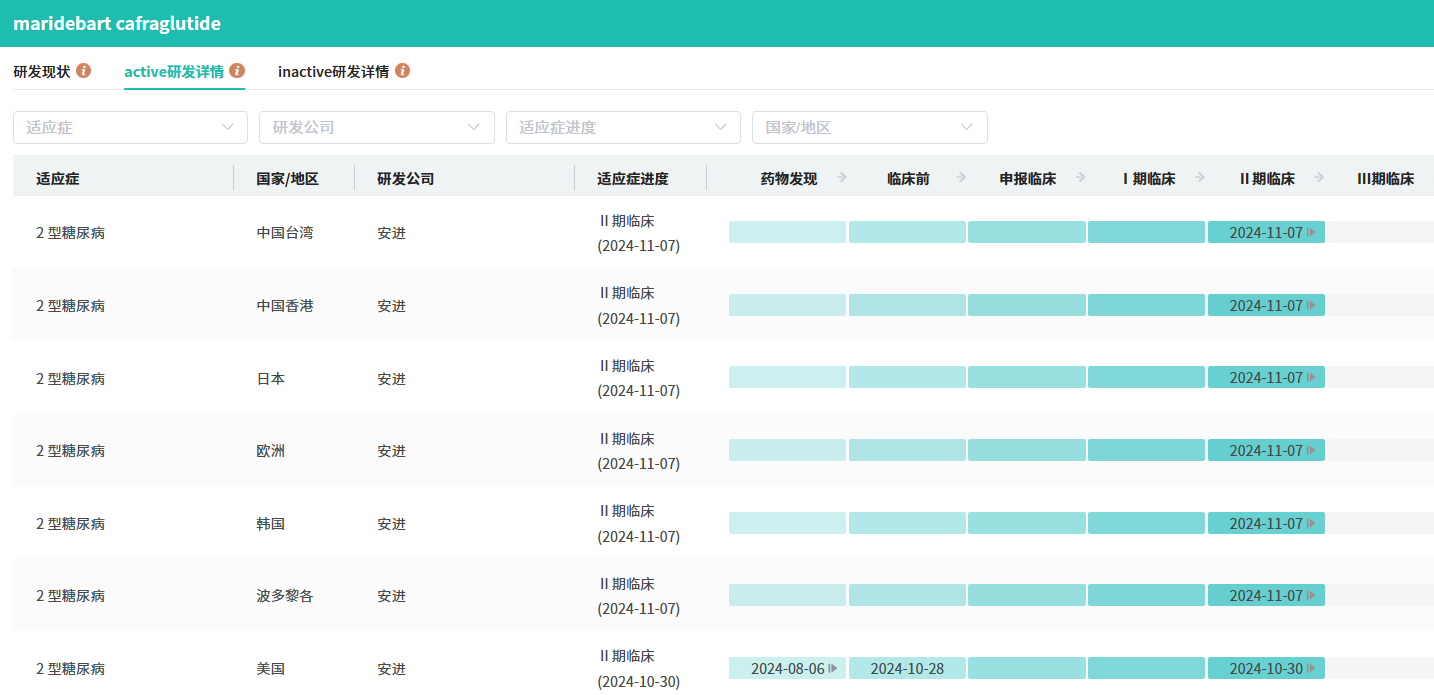
截图来源:摩熵医药全球药物研发数据库
此前在II期研究中,AMG 133已展现出显著的降糖和减重潜力。数据显示,经过52周的治疗,不伴2型糖尿病的肥胖或超重成人患者(n=465,基线平均体重107kg)体重平均下降20%,且未出现体重减轻平台期;而对于伴有2型糖尿病的肥胖或超重成人患者(n=127,基线平均体重104kg,基线平均HbA1c水平7.9%),体重平均降幅达17%,同样未遭遇减重平台期,且平均HbA1c水平显著下降了2.2%。这些积极结果为AMG 133的进一步开发奠定了坚实基础。
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论