
11月2日,礼来制药发布了2023年第三季度财报。报告期内,公司全球销售额为94.99亿美元,同比增长37%,主要得益于Mounjaro、Verzenio 和 Jardiance销售增长的推动以及出售奥氮平组合(Zyprexa)权利带来的14.2亿美元收入。剔除奥氮平组合和 COVID-19 抗体的收入,2023 年第三季度的收入增长了24%。
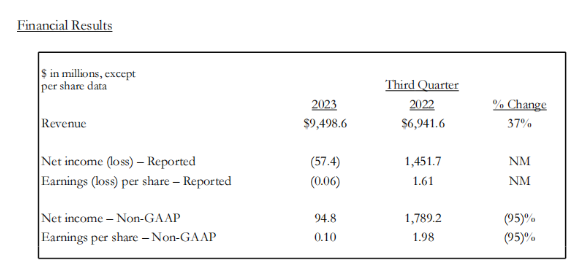
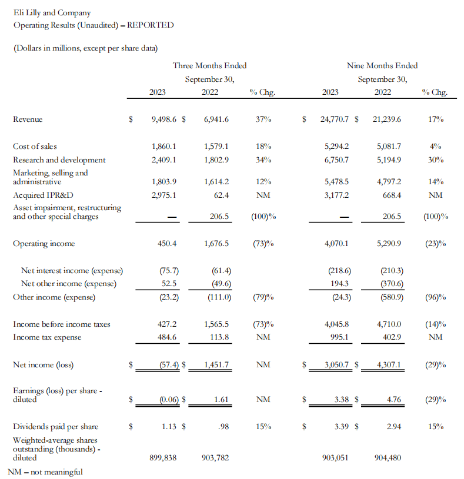
2023年第三季度,研发费用增长了34%,达到24.1亿美元,占收入的25%,主要是由于后期资产的开发费用增加和早期研究的额外投资。2023年第三季度,营销、销售和管理费用增长了12%,达到18亿美元,主要是由于新产品和适应症的相关成本,以及薪酬和福利成本。
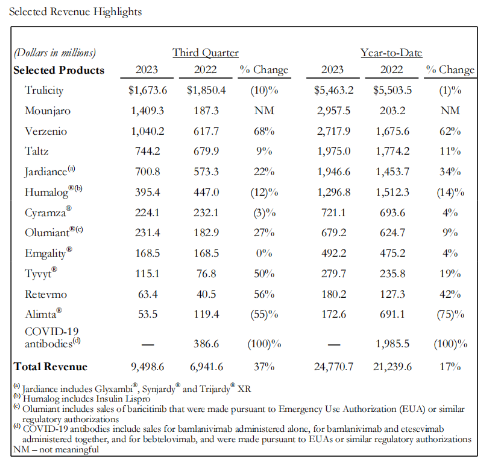
礼来替尔泊肽(Mounjaro)前三季度销售收入总计29.6亿美元(同比+1354%),其中2023Q1销售额为5.7亿美元,2023Q2销售额为9.8亿美元,Q3销售收入为14.1亿美元;长效GLP-1类似物度拉糖肽(Trulicity)前三季度销售收入总计54.6亿美元(同比-1%),Q3销售收入16.73亿美元(同比-10%),公司称销售收入下降的主要原因是这两个季度对回扣和折扣的估算发生了变化。
替尔泊肽基本信息

截图来源:药融云全球药物研发数据库
目前替尔泊肤应用于2型糖尿病适应症在美国、欧洲、日本获批,国内也受理了上市请求。2022年10月,FDA授子替尔泊肤用于成人肥胖或超重的快速通道指定,预计不久后将完成肥胖/超重适应症在美国地区的上市申请滚动递交。
礼来公司最近有关于关键监管、临床、业务发展和其他事件的大量更新,包括:
- 美国食品和药物管理局(FDA)批准Omvoh™(mirikizumab)用于治疗中度和重度活动性溃疡性结肠炎成人患者;
- 美国FDA批准 Jardiance®用于治疗成人慢性肾病;
- 评估米吉珠单抗治疗中度和重度活动性溃疡性结肠炎的安全性和有效性的 VIVID-1 3 期研究结果呈阳;
- LIBRETTO-531的3期临床试验结果呈阳性,与已批准的多激酶抑制剂相比,Retevmo®治在RET突变型甲状腺髓样癌中显示出更高的无进展生存期;
-FDA 对用于治疗早期症状性阿尔茨海默病的 donanemab 采取行动的预期时间更新至 2024 年第一季度;
- 美国FDA根据对第三方生产商的检查结果,对治疗中重度特应性皮炎的 lebrikizumab 签发了完整答复函,未对临床数据包、安全性或标签提出任何问题;
- 完成对DICE Therapeutics、Versanis Bio、Emergence Therapeutics AG和 Sigilon Therapeutics的收购;
- 宣布达成协议收购 POINT Biopharma Global,将肿瘤治疗能力扩展到放射性配体疗法领域 ;
- 宣布公司行政领导团队的变动
参考资料:
礼来第三季度财报
药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论