
3月25日,科伦药业发布公告,其控股子公司科伦博泰自主研发的新型靶向肿瘤相关抗原(TAA)与程序性死亡配体1(PD-L1)的双特异性抗体偶联药物(bsADC)SKB103,已获国家药监局批准开展临床试验,用于治疗晚期实体瘤。

截图来源:企业公告
这是科伦博泰首个进入临床的TAA-PD-L1双抗ADC,也是继SKB571之后该公司在肿瘤治疗领域的第二款进入临床的双抗ADC,标志着公司在ADC技术平台的创新研发又迈出关键一步。
一、创新双抗ADC进入临床,平台化创新能力持续释放
SKB103是科伦博泰基于其专有OptiDC™平台研发的又一款潜力药物。据摩熵医药数据库显示,SKB103在2026年1月12日首次申请临床,3月24日首次获批临床。该药物采用独特设计,有望通过单一分子同时实现两大功能:一是精准递送细胞毒性药物至肿瘤细胞,二是调节肿瘤免疫微环境,从而发挥协同抗肿瘤作用。临床前研究显示,SKB103具有优异的抗肿瘤活性和良好的安全性特征,为后续临床开发奠定了坚实基础。
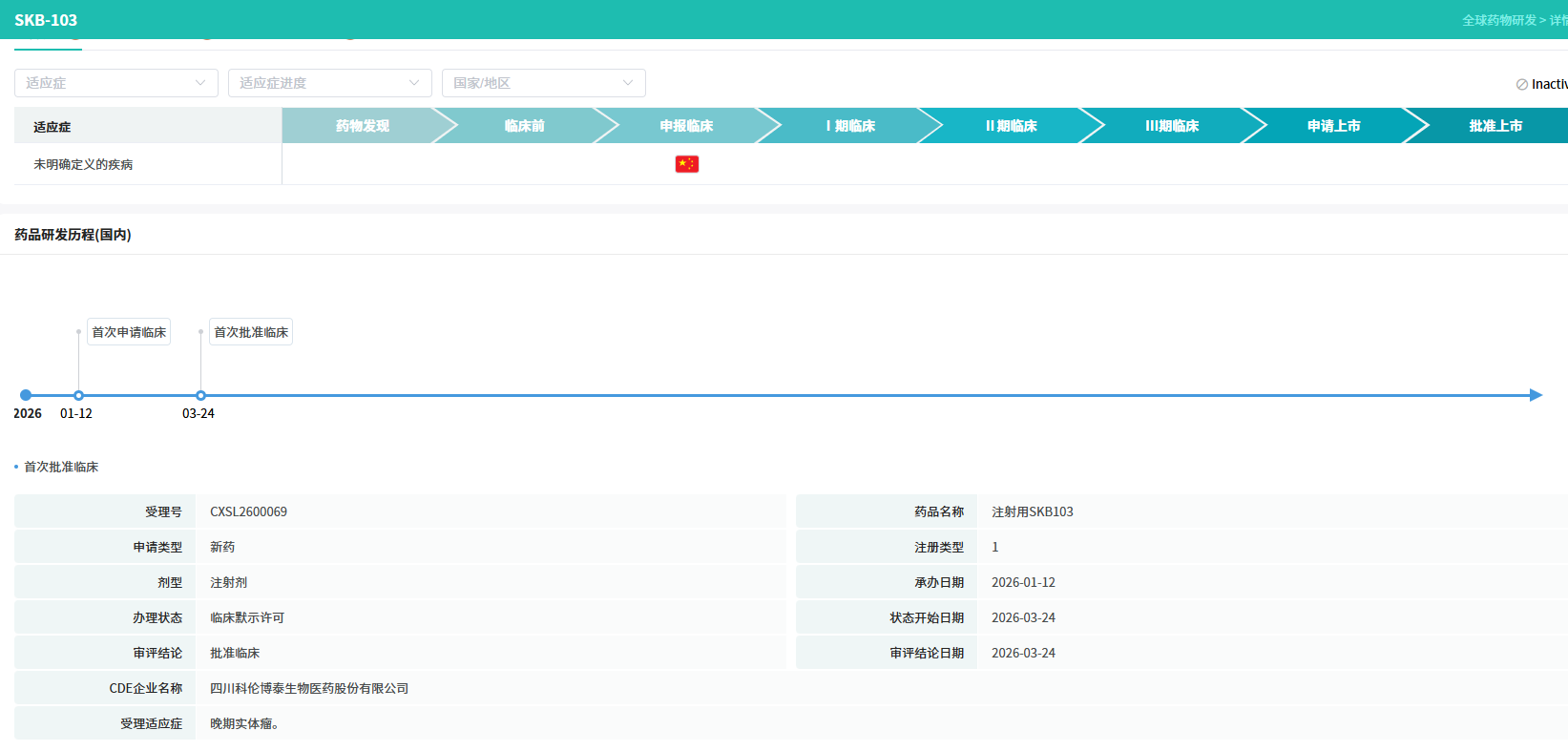
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
科伦博泰在ADC领域已建立起行业领先地位。目前,该公司自主研发的靶向TROP2的ADC和靶向HER2的ADC均已获批上市,并在多个癌种中展现出显著临床疗效。随着SKB103等新一代双抗ADC进入临床,科伦博泰正从单靶点ADC向更复杂的多靶点、多功能ADC药物拓展,构建了涵盖放射性核素偶联药物、双抗ADC等前沿技术的多元化管线矩阵。
二、2025年实现20亿营收,药品收入激增950%
2025年,科伦博泰迎来商业化的重要转折点。全年实现总收入20.58亿元,同比增长6.5%。其中,药品销售收入从2024年的5170万元猛增至5.43亿元,增幅高达950%,成为公司增长的核心引擎。
这一爆发式增长主要得益于两款核心ADC产品的成功商业化:
- 芦康沙妥珠单抗(靶向TROP2 ADC):作为国内首个获得完全上市许可的国产ADC,已在三阴性乳腺癌、HR+/HER2-乳腺癌及非小细胞肺癌等多个适应症获批,并于2025年底成功纳入国家医保目录。
- 博度曲妥珠单抗(靶向HER2 ADC):作为首个在中国获批的国产HER2 ADC,用于HER2阳性乳腺癌治疗,进一步巩固了公司在ADC领域的领先地位。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论