
10月17日,据国家药品监督管理局(NMPA)官网最新公示,科伦药业旗下科伦博泰申报的1类新药注射用博度曲妥珠单抗在国内获批上市;与此同时,科伦药业按化药注册分类4类申报的罗替高汀贴片也获批上市,且视同通过一致性评价,一举拿下国内首仿。
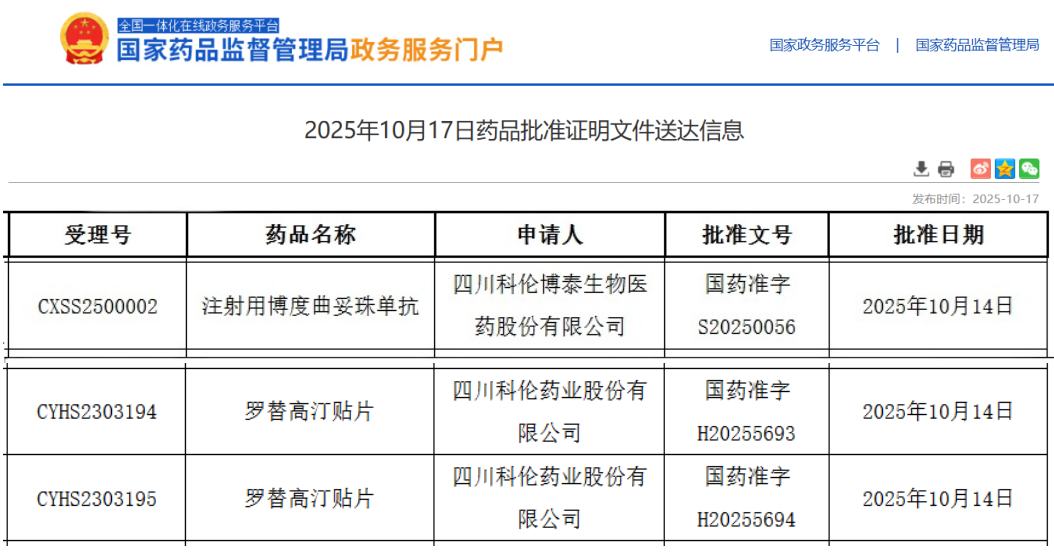
截图来源:NMPA
2款ADC药物已上市,9款处于I期临床及以上
注射用博度曲妥珠单抗是科伦博泰自主研发的HER2 ADC单抗,适用于既往接受过一种及以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。该药于2017年首次在国内申报临床,2018年启动首个临床试验。2023年5月,科伦博泰提交的首个上市申请(针对既往经二线及以上抗HER2治疗失败的HER2阳性不可切除局部晚期、复发或转移性乳腺癌)获CDE受理,目前仍在审评中;本次获批适应症为该药第二项上市申请,于2025年1月获CDE受理。
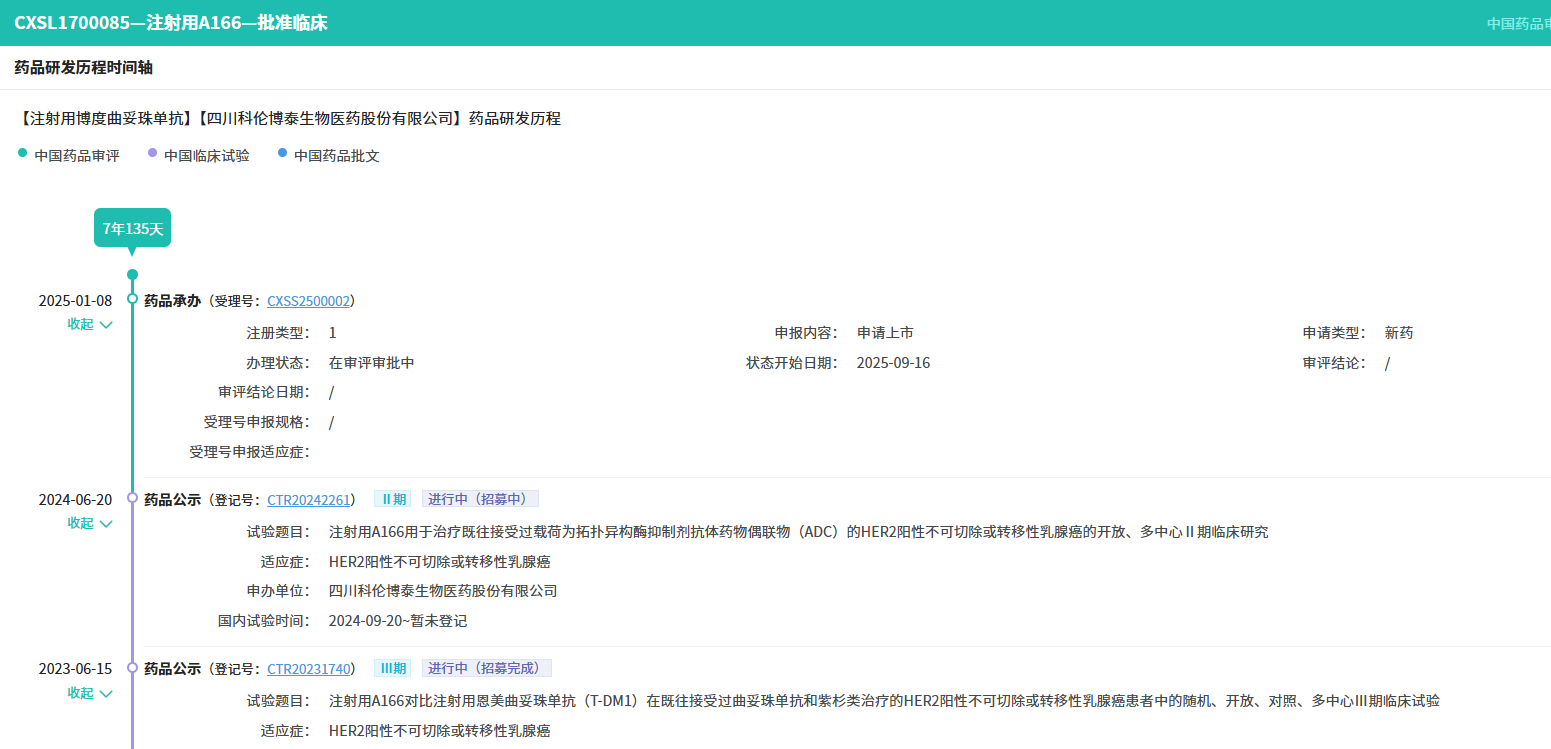
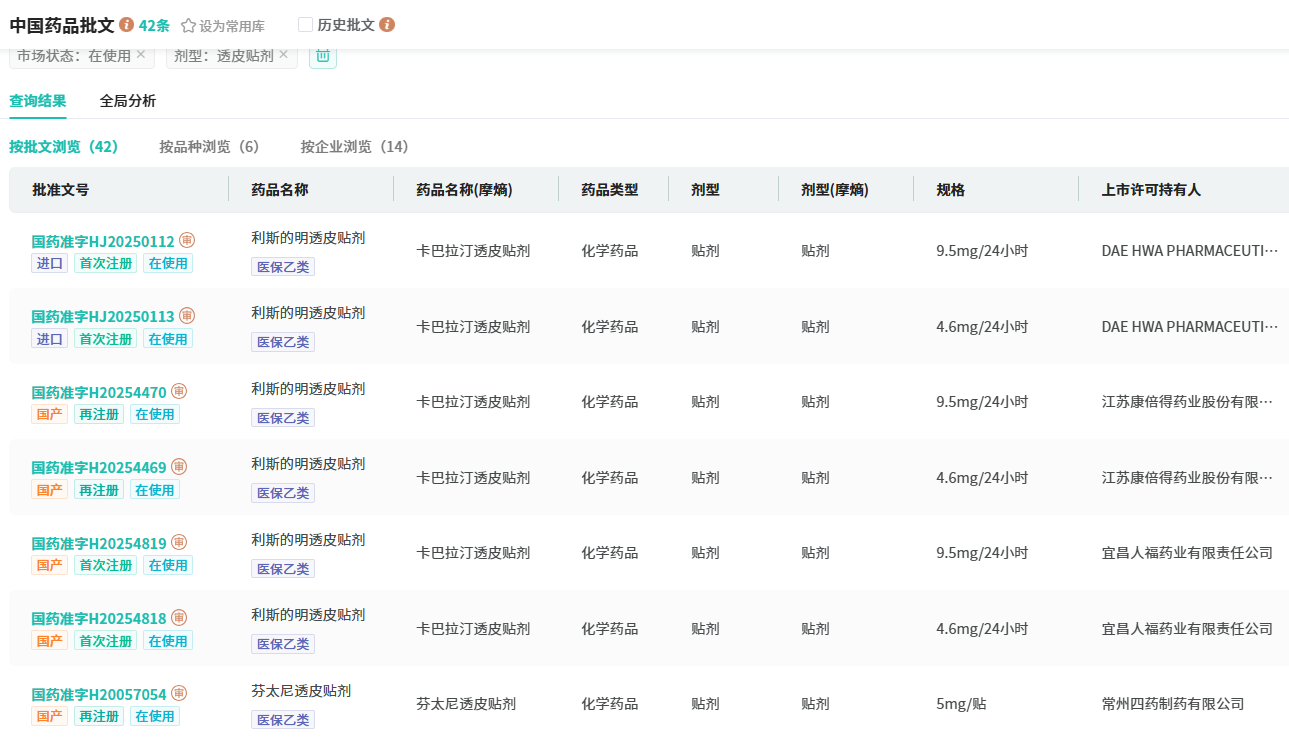
截图来源:摩熵医药中国药品审评数据库
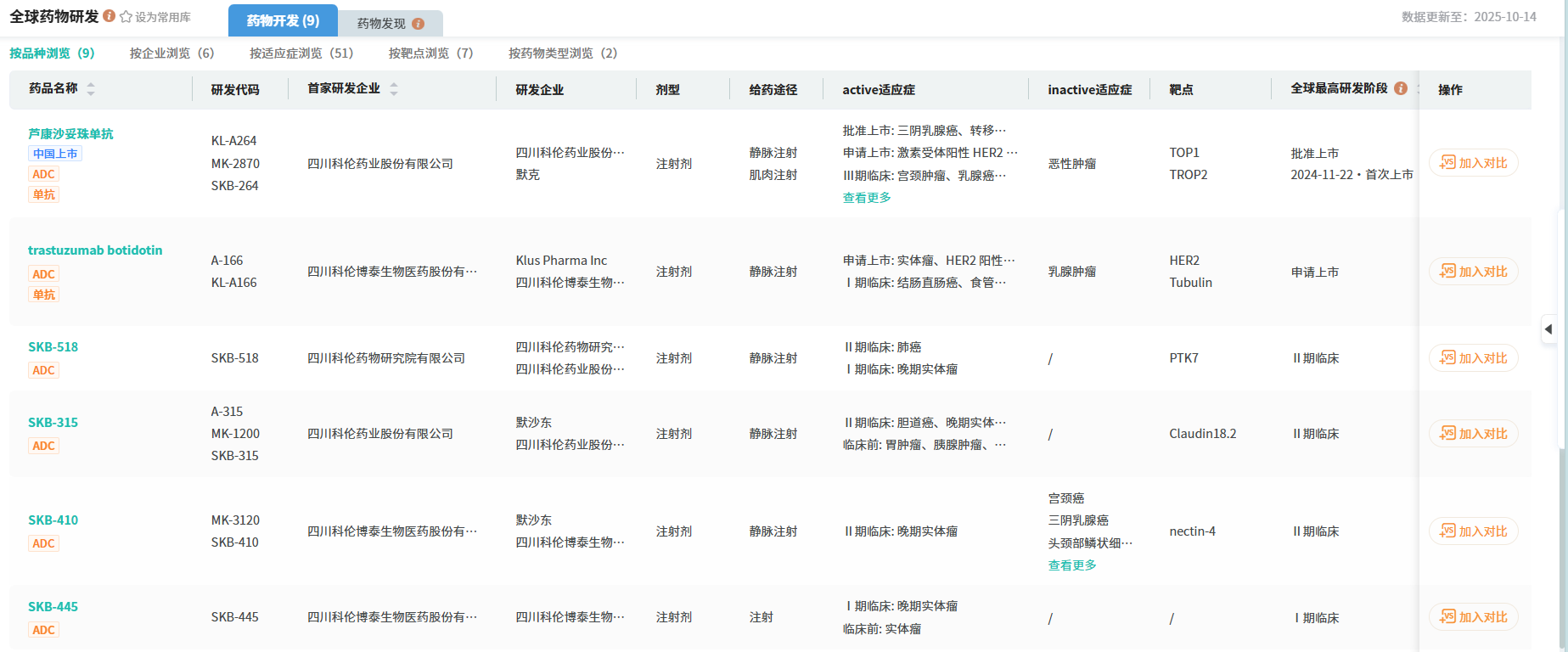
目前,全球已获批的5款原研HER2 ADC均在国内获批。ADC药物是科伦药业重点布局方向,据摩熵医药数据库显示,旗下已有芦康沙妥珠单抗、博度曲妥珠单抗2款新药获批上市。此外,科伦药业(含子公司)有9款ADC药物处于I期临床及以上阶段,涵盖新型双抗ADC药物SKB571,以及SKB518、SKB-410、SKB-500等ADC新药。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论