
4月16日,强生(J&J)宣布决定将失败的基因疗法botaretigene sparoparvovec(简称bota-vec)退还给MeiraGTx,后者以2500万美元首付将这一曾在III期临床折戟的资产重新收入囊中。

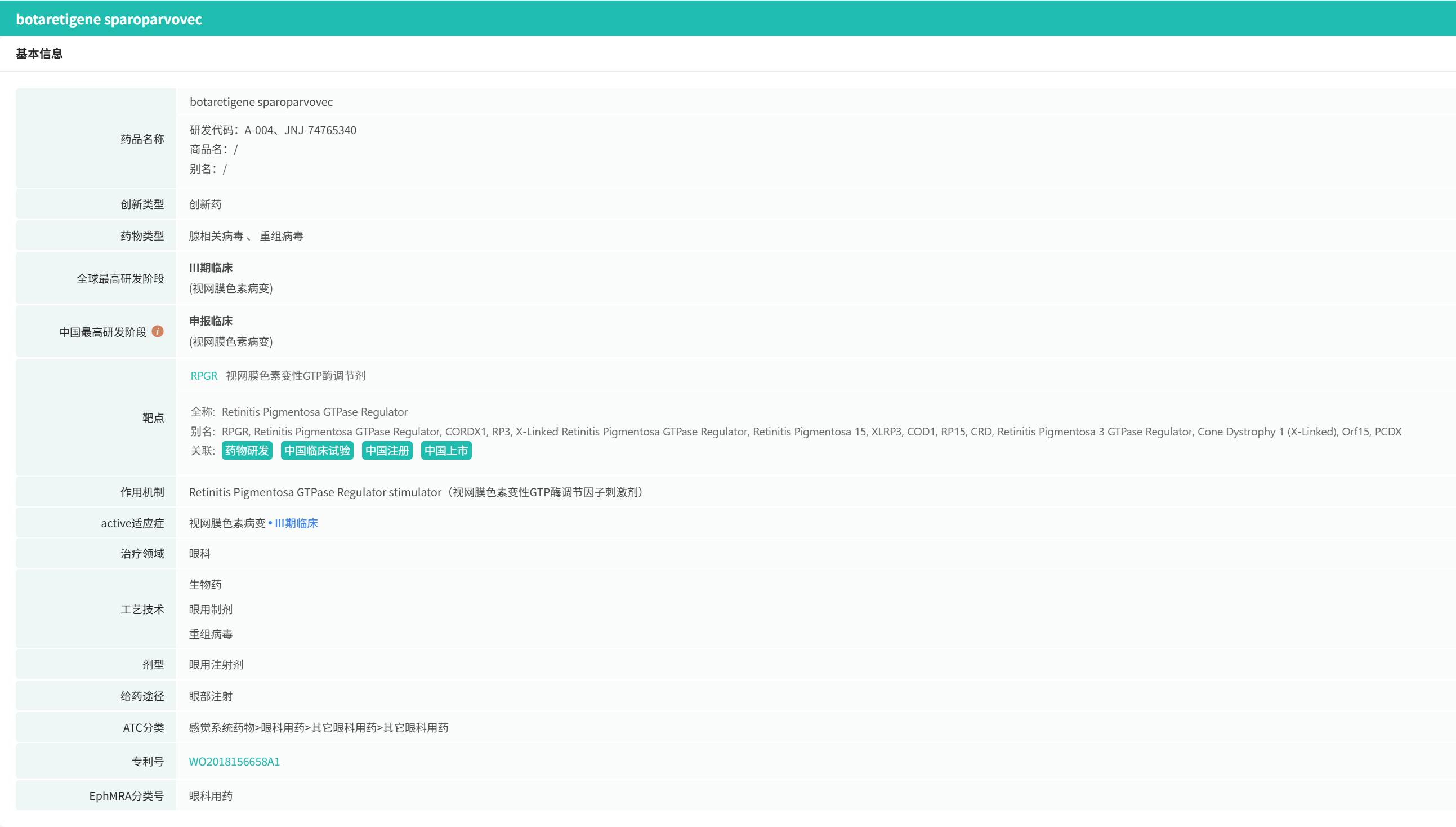
查数据,找摩熵!图源:摩熵医药数据库
这笔交易的金额与其说是"回购",不如说是大药企止损离场后,biotech对自身技术平台的最后一搏。
MeiraGTx与强生的这段合作始于2023年底。强生旗下杨森制药以最高4.15亿美元的潜在交易金额,获得bota-vec的全球开发及商业化权利,首付款项约1亿美元。
彼时,该AAV基因疗法正处于III期临床研究阶段,用于治疗X连锁视网膜色素变性(XLRP),市场对其充满期待。
XLRP是一种主要影响男性的罕见遗传性眼病,由RPGR基因突变引起,患者通常在青少年时期开始出现夜盲症状,40岁左右便面临法定失明。基因疗法被认为是有望从根本上延缓疾病进展的潜在治愈手段。
然而,2025年5月公布的III期临床试验结果给这一期望泼了冷水。
bota-vec未能达到主要终点,即改善XLRP患者视力引导行动能力的主要功能性指标。这一失败直接导致强生决定退还该资产。
MeiraGTx随即以2500万美元首付、加上里程金和销售分成的形式,将全部权利收回。公司表示,仍计划在美国和欧盟寻求加速批准,目标是2027年上市。
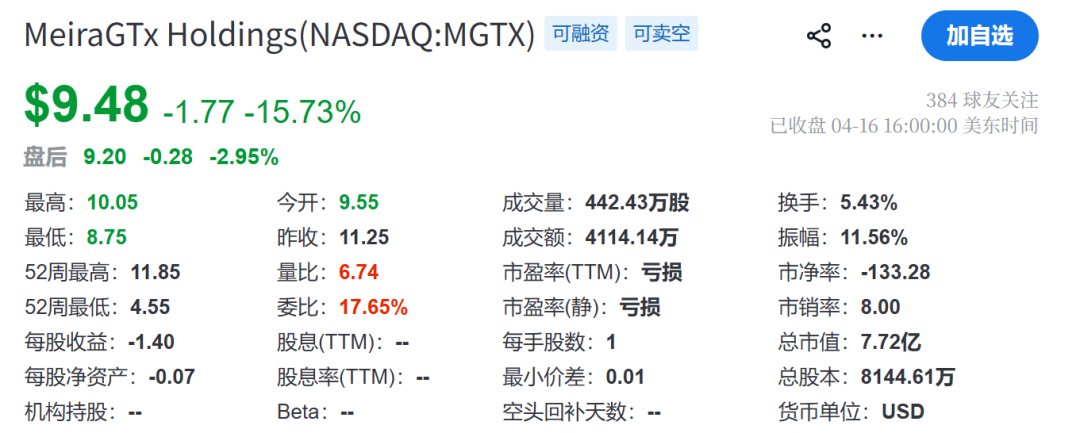
受此消息影响,MeiraGTx股价单日下跌近16%,反映出投资者对这一决定的疑虑。
眼科是基因治疗商业化最为成熟的疾病领域。2017年获FDA批准的Luxturna(voretigene neparvovec)由Spark Therapeutics开发、后来被罗氏收购,是全球首个获批的眼科基因疗法,用于治疗RPE65基因突变相关的遗传性视网膜疾病。
Luxturna的定价一度高达85万美元/双眼,是历史上最昂贵的药物之一。尽管商业化表现平平,但其获批本身为整个领域奠定了监管基础。
在XLRP赛道上,除了bota-vec,还有Biogen的timrepigene emparvovec以及Nightstar Therapeutics的AAV2-REP1等项目处于研发中。Nightstar于2019年被渤健以约8亿美元收购,但此后多个项目遭遇挫折,渤健最终在2024年宣布放弃眼科基因治疗业务。
MeiraGTx宣布将继续寻求加速批准的背景,是FDA生物制品审评与研究中心(CBER)即将迎来人事变动。现任负责人Vinay Prasad宣布将于2025年离任,这一消息在基因治疗行业引发广泛关注。Prasad在任期间对基因疗法的审批态度相对开放,推动了多款创新疗法的加速获批,但其倡导的以随机对照试验为金标准的主张也引发过争议。
加速批准路径对基因治疗领域尤为重要。由于罕见病患者群体小、入组困难,传统临床试验设计面临挑战。加速批准允许基于替代终点批准上市,后续验证性研究补充疗效证据。
然而,这一通道正在收窄的风声已在业内流传。新任监管者的态度将直接影响bota-vec等处于审评阶段项目的命运。MeiraGTx能否在2027年实现商业化目标,很大程度上取决于监管环境的演变。
关于MeiraGTx
MeiraGTx Holdings是一家垂直整合的临床阶段基因治疗公司,有四个正在进行的临床项目和一系列临床前和研究项目。在病毒载体设计和优化,基因疗法制造以及潜在的转基因基因调控技术方面拥有核心能力。2023年获赛诺菲投资,2025年与国际制药巨头礼来(Eli Lilly) 达成一项总金额高达4.75亿美元的战略合作,共同推进针对Leber先天性黑矇4型 (LCA4) AAV基因疗法 (rAAV8.hRKp.AIPL1) 的后续开发和商业化。
MeiraGTx Holdings管线

参考来源:
[1] 企业官网/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 强生/MeiraGTx开发治疗视网膜色素变性的眼部基因疗法,显著改善视觉功能
2. 强生2026年Q1业绩炸裂:总营收241亿美元,肿瘤业务狂飙23%,上调全年指引至千亿级
3. 强生2026年战略解码:跨越Stelara专利悬崖,AI+量子计算驱动千亿营收新帝国
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论