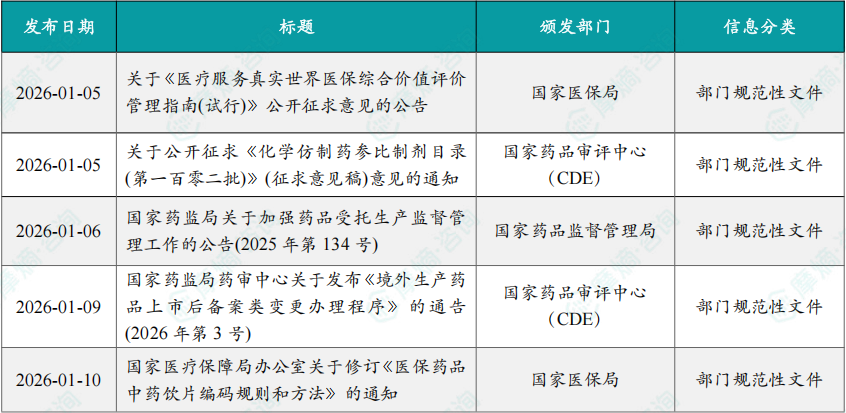
1.3.1 本周国内医药大健康行业政策法规速览
1.3.2 本周重点行业政策详细说明
·国家药监局发布《关于加强药品受托生产监督管理工作的公告》
1月6日,国家药监局发布《关于加强药品受托生产监督管理工作的公告》,自发布之日起执行。《公告》支持创新药、临床急需药品等品种开展委托生产,鼓励参与研发并实现品种上市、具备相应生产能力、高水平、专业化的合同研发生产型受托生产企业(CDMO)发展,支持其接受委托生产,支持同一集团内执行统一质量管理体系的企业之间委托生产药品,并在《公告》相关条款中明确了具体的支持政策。通过这些措施,引导质量管理水平高的持有人和专业化的CDMO企业开展委托生产,进一步保障药品质量安全,促进创新产品上市,满足公众用药需求。
《公告》主要包括强化受托生产企业责任、加强受托生产监督管理和其他事项三个部分的内容,并以附件形式对《药品受托生产意见书》申请资料、出具要求和出具模板予以明确。
一是强化受托生产企业责任。《公告》明确了受托生产企业的总体要求及应当具备的条件,强调受托生产企业接受委托前应当对持有人及受托生产产品进行评估,并进一步细化了受托生产企业在技术转移、风险防控、质量管理体系衔接、质量信息沟通、共线生产管理、变更管理、留样和稳定性考察、产品放行等方面的要求。
二是加强受托生产监督管理。《公告》明确了委托和受托药品生产许可事项办理程序及委托生产许可时限管理要求,进一步细化了无菌药品等高风险产品委托生产、长期停产品种恢复生产等管理要求,要求省级药品监管部门强化药品委托双方企业关键人员履职能力的考核评估、依据风险强化检查和抽检、做好跨省监管协作和违法行为查处等工作。
三是其他事项。明确《公告》发布后的执行和整改要求;明确支持鼓励创新药、临床急需药品等委托生产,鼓励委托双方采用生产质量信息化管理系统,推动产业深度转型升级,鼓励发展新质生产力。
同期事件:
1. 2026年第2周01.05-01.11国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第2周01.05-01.11国内仿制药/生物类似物申报/审批数据分析
3. 2026年第2周01.05-01.11全球创新药研发概览
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.01.05-2026.01.11) },如需查看或下载完整版报告,可点击!
扩展阅读:
1. 2024年第38周09.16-09.22国内医药大健康行业政策法规汇总
2. 2024年第32周08.05-08.11国内医药大健康行业政策法规汇总
3. 2024年第26周06.24-06.30国内医药大健康行业政策法规汇总
查数据,找摩熵!想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论