
2月22日,CDE官网公示,信达生物申报的信迪利单抗注射液和伊匹木单抗注射液联合疗法获得受理。该联合疗法此前已被纳入优先审评,适应症为两药联合用于可切除的微卫星高度不稳定型(MSI-H)或错配修复缺陷型(dMMR)结肠癌患者的新辅助治疗。
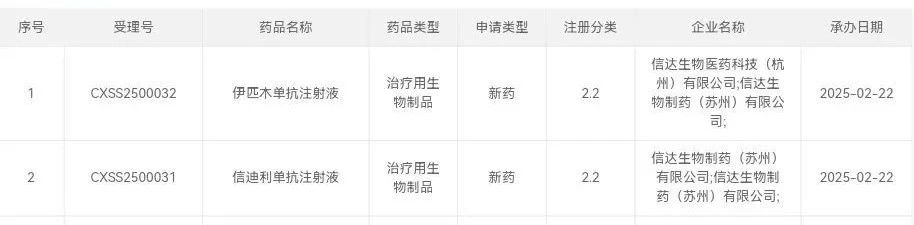
截图来源:CDE
据摩熵医药数据库显示,信迪利单抗是一种 PD-1 抑制剂,已在国内获批 8 项适应症,涵盖经典型霍奇金淋巴瘤、非鳞状非小细胞肺癌、鳞状非小细胞肺癌、肝细胞癌、食管鳞癌、胃及胃食管交界处腺癌、子宫内膜癌多个癌种。
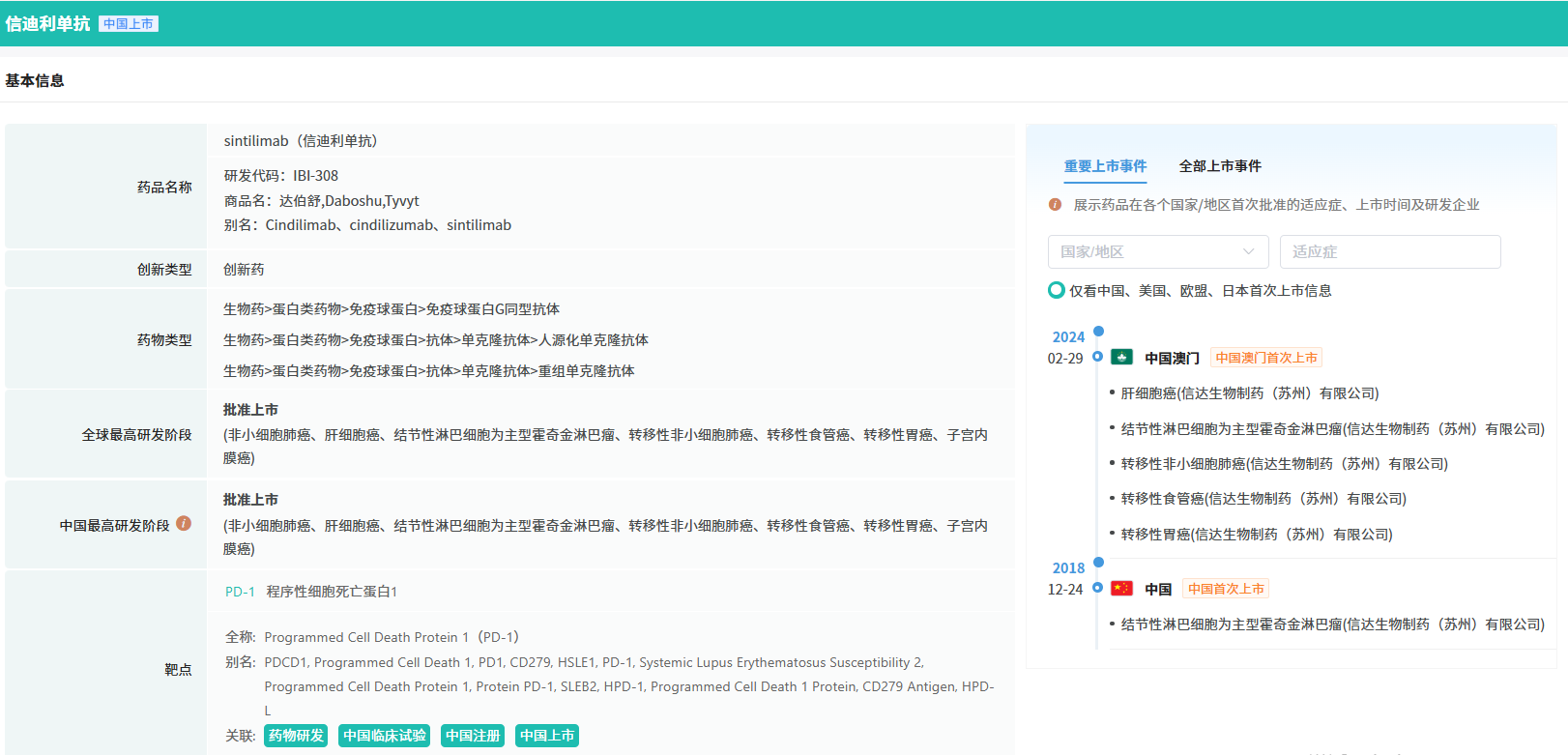
截图来源:摩熵医药全球药物研发数据库
伊匹木单抗(IBI310)是信达开发的一种抗 CTLA4 单抗,它能特异性结合 CTLA-4,从而阻断 CTLA-4 介导的 T 细胞抑制,促进 T 细胞的激活和增殖,提高肿瘤免疫反应,达到抗肿瘤的效果。IBI310 尚未获批,国内最高研发进度是 Ⅲ 期临床。
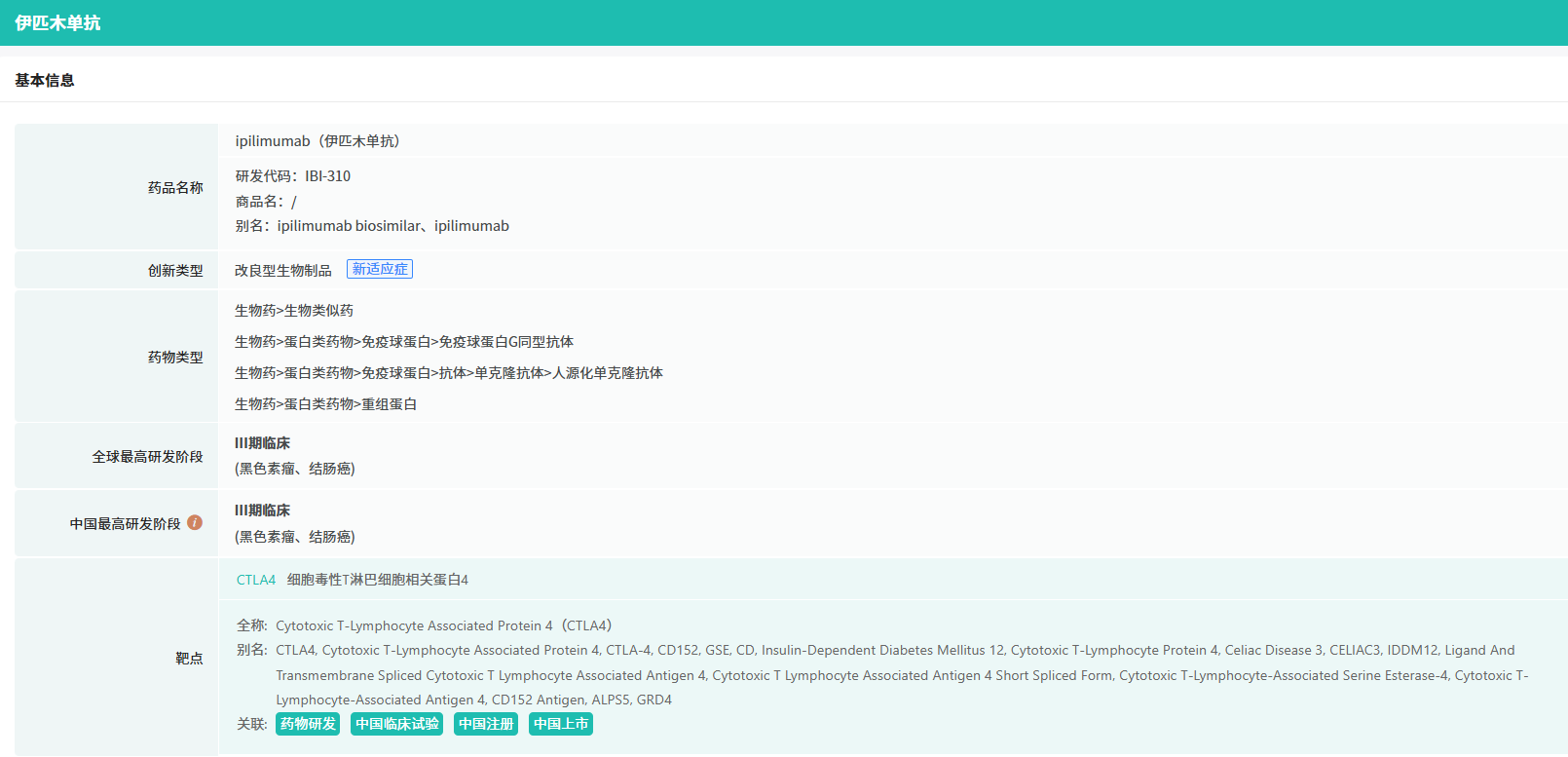
截图来源:摩熵医药全球药物研发数据库
本次申报上市的是这两款药物的联合疗法,适应症是可切除的 MSI-H/dMMR 结肠癌患者的新辅助治疗。
信达生物在新闻稿中表示,目前部分IIB-III期结肠癌的根治性手术难度大,创伤范围广,部分患者难以达到完全(R0)切除,预后较差。而在MSI-H/dMMR结肠癌中新辅助化疗的疗效欠佳, pCR率仅有约5%。IBI310联合信迪利单抗新辅助治疗有望改变临床实践,能够降低术前分期,缩小根治性手术切除范围,提高完全切除率,减少术后辅助化疗的需要,降低复发率,从而改善长期预后潜力。
本次IBI310联合信迪利单抗申报上市并被纳入优先审评,意味着这款联合疗法有望加速获批,惠及患者。
参考来源:
[1] CDE官网
[2] 摩熵医药(原药融云)数据库
[3] 信达生物官方披露
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论