
10月11日,据中国国家药品监督管理局(NMPA)官网最新公示,广东东阳光药业按化药注册分类申报的盐酸芬戈莫德胶囊获批上市,并拿下国内首仿。目前,东阳光药业是该产品首家申报仿制上市并获批的国内药企,同时也是该公司首款口服免疫抑制剂。

截图来源:NMPA
芬戈莫德是诺华从日本Mitsubishi制药引进的药物,在2010年9月在美获批,成为首个可经口服给药的用于复发缓解型多发性硬化症的治疗,是同类药物中首个可口服的新型免疫抑制剂。盐酸芬戈莫德胶囊被纳入国家第一批临床急需药品名单,原研在2019年获批进入中国市场,随后在2020年进入国家医保谈判目录,现为2024版国家医保常规目录品种。
芬戈莫德上市初期,全球市场表现不错。2018年超33亿美元的销售成绩。据摩熵医药数据库显示,该药品在2024年全球市场的销售额超5亿美元。
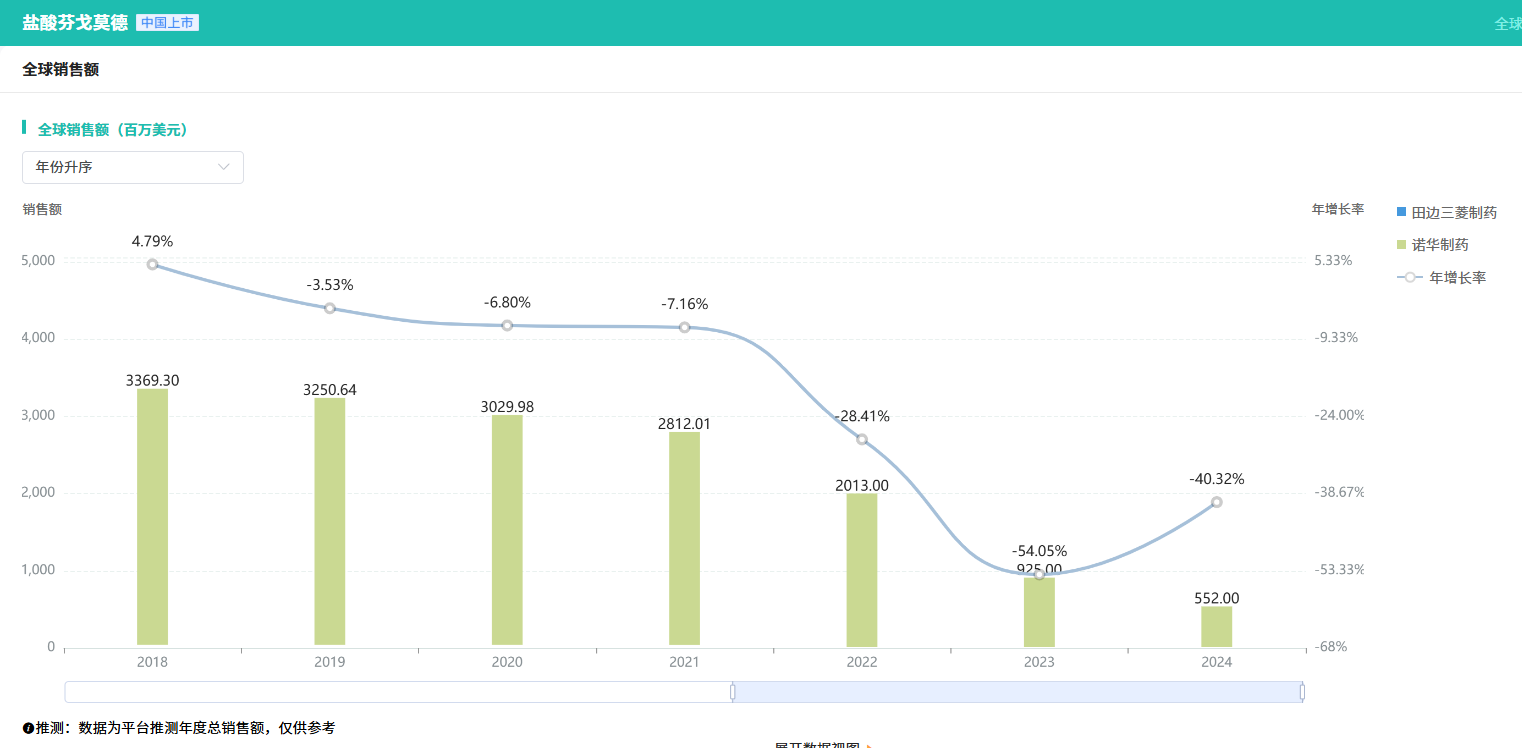
截图来源:摩熵医药全球药物研发数据库
东阳光药业是国内较早布局芬戈莫德产品的药企之一,该项目2011年7月立项,分别在中国、美国和欧盟申报,其中欧洲(西班牙、德国和意大利)和美国已经获批;国内市场,广东东阳光药业在2020年首家申报仿制上市,并在近期获批国内首仿+首家过评,打破了原研药独霸的局面。
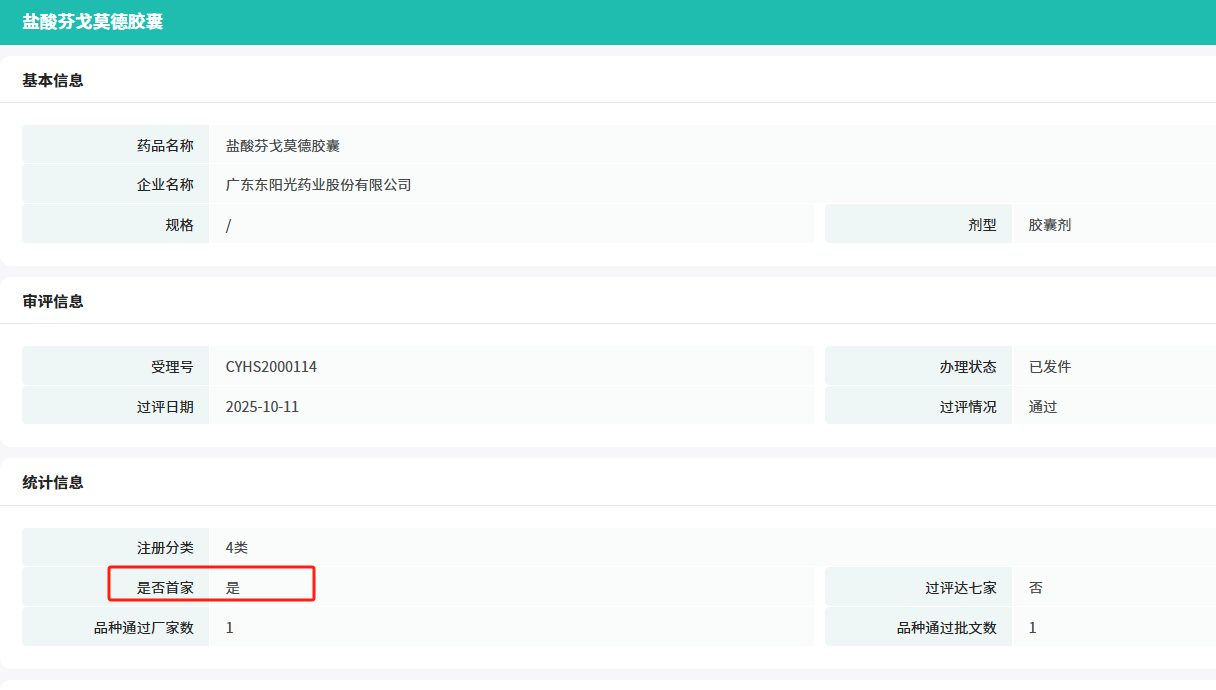
截图来源:摩熵医药过评药品汇总数据库
在产品布局层面,当前盐酸芬戈莫德胶囊在国内的申报情况呈现出特定态势。仅印度瑞迪博士实验室的进口5.2类申报产品处于审评审批阶段,尚未有新的突破性进展。
截至目前,广东东阳光药业有18款品种迎来过评,其中氢溴酸加兰他敏口腔崩解片、艾司奥美拉唑镁肠溶胶囊、利格列汀片等7款品种为首家过评。此次盐酸芬戈莫德胶囊获批,是公司首款口服免疫抑制剂。
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论