
10月20日,石药集团宣布,旗下附属公司上海津曼特生物科技与江苏康宁杰瑞生物制药合作开发的 JSKN003(一种靶向HER2双表位的抗体偶联药物)再次获国家药监局授予突破性治疗认定,拟定适应症为单药用于既往经奥沙利铂、氟尿嘧啶和伊立替康治疗失败的HER2阳性晚期结直肠癌患者的治疗。

截图来源:企业公告
结直肠癌是全球最常见的恶性肿瘤之一。根据国际癌症研究机构(IARC)的统计数据,2022年全球结直肠癌新发病例192.62万例,死亡病例90.39万例,其发病率及死亡率分别位列全部恶性肿瘤的第3位和第2位。在中国,结直肠癌尤其高发,其发病率仅次于肺癌,位居第2位,每年新发病例超过50万例,且逐年上升。
对于既往经奥沙利铂、氟尿嘧啶和伊立替康治疗失败的HER2晚期结直肠癌患者,国内已获批药物包括瑞戈非尼、呋喹替尼及曲氟尿苷替匹嘧啶,但这些药物的疗效十分有限,中位无进展生存期(mPFS)仅为2~3.7个月,中位总生存期(mOS)为7~10个月左右。因此,该患者人群仍存在着巨大的未被满足的临床需求。JSKN003 在该适应症人群中的初步临床研究结果显示出突出的疗效和良好的安全性,与现有治疗手段相比具有显著的临床优势。
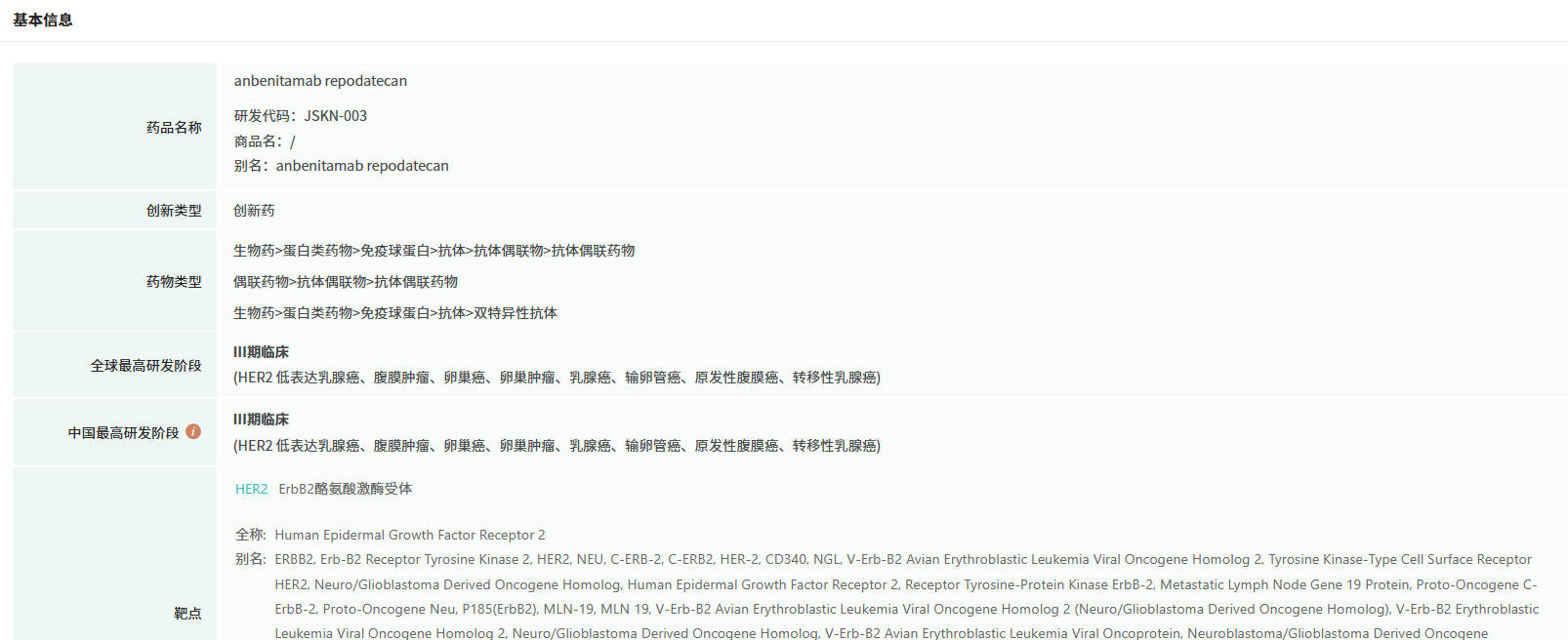
截图来源:摩熵医药数据库-全球药物研发数据库
此前,JSKN003 针对不限HER2表达水平的铂耐药卵巢癌适应症已获得CDE突破性疗法认定、美国食品药品监督管理局(FDA)临床研究许可,胃癌及胃食管结合部癌适应症已获得美国FDA孤儿药资格认定。
该适应症为 JSKN003 获授予的第二项突破性治疗认定。于2025年3月,JSKN003 用于治疗铂耐药复发性上皮性卵巢癌、原发性腹膜癌或输卵管癌适应症亦获国家药监局授予突破性治疗认定。目前,JSKN003 正在中国开展用于治疗乳腺癌、卵巢癌、胃癌等实体瘤的多项II期及III期临床研究。

截图来源:摩熵医药全球药物研发数据库
JSKN003 再次获授予突破性治疗认定,将进一步加快该产品的研发和审评速度,以期及早惠及更多肿瘤患者。
参考来源:
[1] 企业公告
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 石药集团:最新ADC产品SYS6023获得美国临床试验批准!
3. 石药集团捷报频传!130款创新药在研,120+品种过评,26款品种备战第十批集采!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论