1月20日,恒瑞医药递交的3类仿制药「尼莫地平口服溶液」获批上市,勇夺该品种的国内首仿+首家过评,也将成为2022年继「盐酸氨溴索口服溶液」后,恒瑞医药过评的第2款药品和口服液体剂。据查询,目前国内仅有24款口服液体剂过评。恒瑞医药近几日捷豹频传,双喜临门!其PD-L1 单抗「阿得贝利单抗」报上市的申请也于1月19日获受理,是我国第五款报上市的PD-L1单抗。(《国产PD-L1单抗第5款报上市,来自恒瑞医药!产品收获颇丰!》)
尼莫地平口服液获批


截图来源:NMPA官网
阿得贝利单抗申报上市

截图来源:CDE官网
5亿心血管大品种,恒瑞医药拿下首仿!
尼莫地平属于第二代地平类药物,是临床常用的抗高血压药物。据药融云数据统计,尼莫地平近年的院内销售额稳定在5亿元上下。2021前三季度,院内销售已超5亿,同比增长38%,其中,原研拜耳的市场占比最大(近6成),具体产品方面,以尼莫地平注射液为主力。
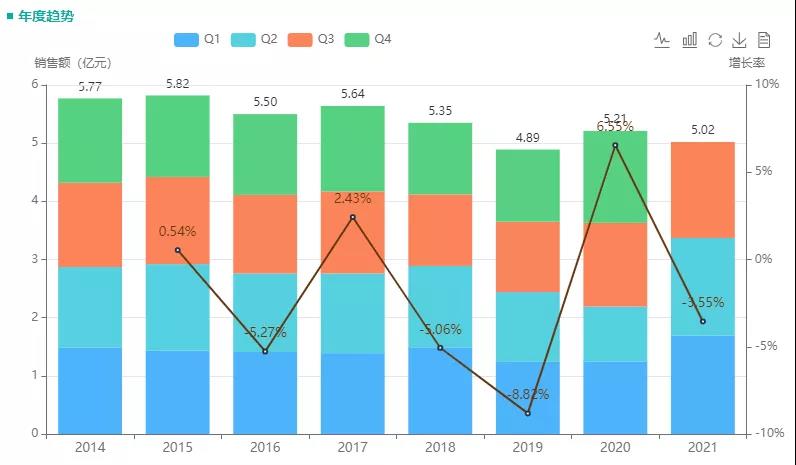
截图来源:药融云全国医院销售数据库
目前尼莫地平在国内获批生产的剂型有普通片剂、胶囊剂、注射剂等,其中仅尼莫地平注射液尚无产品过评。此次恒瑞医药的尼莫地平口服溶液过评,为该品种首仿+首家过评,此外,还有广东金城金素制药/浙江康恩贝制药和浙江国镜药业以仿制3类报产该品种。
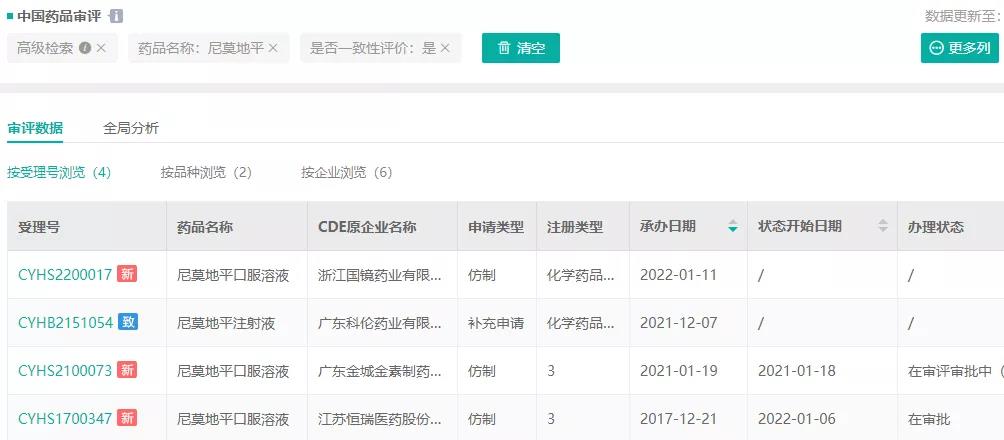
截图来源:药融云中国药品审评数据库
阿得贝利单抗:有望成国内第7款获批的PD-L1单抗
在此前国内已有4款PD-L1单抗上市,2款申报上市。恒瑞医药阿得贝利单抗有望成为国内第7款获批的PD-L1单抗。截至目前,恒瑞医药在该药已经投入超2亿元。
根据药融云中国药品批文最新数据显示,国内已上市的PD-L1 单抗有阿斯利康的度伐利尤单抗注射液、罗氏的阿替利珠单抗注射液、康宁杰瑞的恩沃利单抗注射液和基石药业的舒格利单抗注射液。

数据来源:药融云企业版中国药品批文,https://db.pharnexcloud.com/
截至目前,尚无PD-L1单抗纳入2022医保。在获批适应症数量方面,罗氏的阿替利珠单抗注射液有着不小优势。
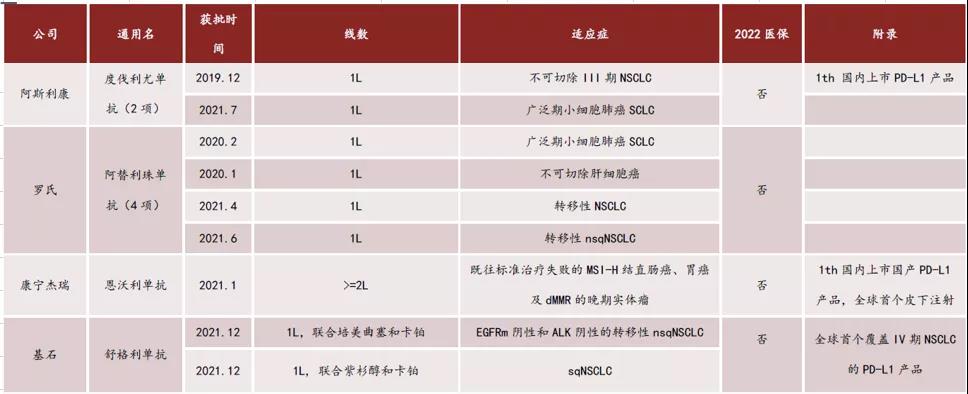
来源:莫尼塔研究
阿得贝利单抗(SHR-1316)相关临床试验
阿得贝利单抗(SHR-1316)是恒瑞医药自主研发的人源化抗 PD-L1 单克隆抗体,能通过特异性结合 PD-L1 分子从而阻断导致肿瘤免疫耐受的 PD-1/PD-L1 通路,重新激活免疫系统的抗肿瘤活性,从而达到治疗肿瘤的目的。在药融云中国临床试验数据库中,可以查询到SHR-1316的11条临床试验信息。
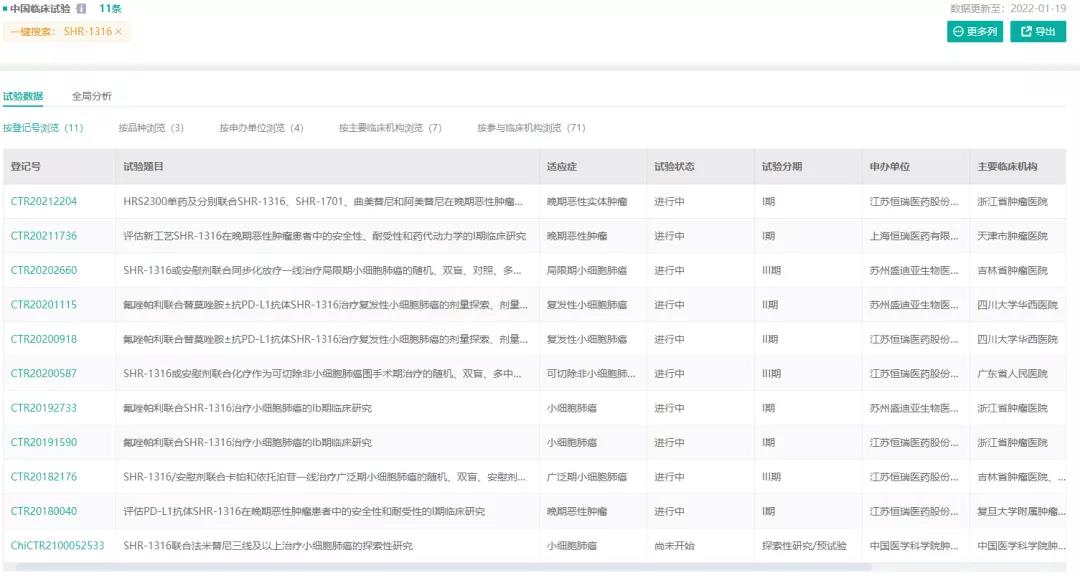
截图来源:药融云中国临床试验
2021年10月27日,恒瑞医药宣布,其1类新药PD-L1单抗SHR-1316(阿得贝利单抗注射液)联合化疗一线治疗广泛期小细胞肺癌的随机、双盲、安慰剂对照、多中心的III期临床研究(SHR-1316-III-301)主要研究终点结果达到方案预设的优效标准。研究结果表明,SHR-1316 联合化疗对比安慰剂联合化疗可以显著延长患者生存(OS)。

SHR-1316-III-301研究是一项评估SHR-1316(阿得贝利单抗注射液)或安慰剂联合依托泊苷和卡铂用于广泛期小细胞肺癌一线治疗有效性和安全性的随机、双盲、III期对照临床研究。这项试验由吉林省肿瘤医院程颖教授和中国医学科学院肿瘤医院王洁教授共同担任主要研究者。全国49家中心共同参与,主要研究终点是总生存期(OS),次要研究终点包括无进展生存期(PFS)、客观缓解率(ORR)、缓解持续时间(DoR)、疾病控制率(DCR)和安全性等。
市场前景广阔,PD-(L)1领域恒瑞医药将稳坐国内龙头
手握PD-1和PD-L1重磅大品种,恒瑞医药在PD-(L)1领域销售额有望突破70亿。恒瑞医药PD-1单抗卡瑞利珠单抗,2021年销售额业内预计接近50亿元。PD-L1单抗如果获批,凭借恒瑞医药在肿瘤领域的成熟销售渠道,将快速放量,销售额峰值有望达到20亿元。
结语
PD-(L)1目前国产企业布局研发的项目已经突破了100个,涉及单抗、双抗、小分子化药等多个领域。扎堆内卷已经成了PD-(L)1无法避免的话题,拼研发速度成了脱颖而出的关键。面对如此多的同靶点新药,CDE在批准一定数量后,收紧审评审批肯定在所难免。研发有风险,立项需谨慎。
—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论