
3月3日,CDE官网显示,礼来(Eli Lilly)提交的 来瑞奇珠单抗注射液 上市申请获受理,注册分类为3.1类。该药物是首款在国内递交上市申请的IL-13单抗。这意味着,继 度普利尤单抗 之后,又一款全球重磅IL-13抑制剂有望登陆中国市场,为饱受瘙痒与皮损困扰的患者带来新的选择。
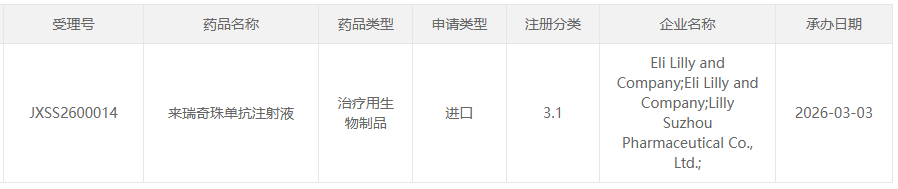
截图来源:CDE官网
一、机制解码:精准阻断IL-13,直击特应性皮炎“炎症枢纽”
来瑞奇珠单抗(Lebrikizumab)是一款高亲和力、选择性靶向白细胞介素-13(IL-13)的单克隆抗体。IL-13是特应性皮炎发病的核心细胞因子,可直接驱动皮肤中的2型炎症反应循环,导致皮肤屏障受损、顽固瘙痒、角质层增厚及继发感染。
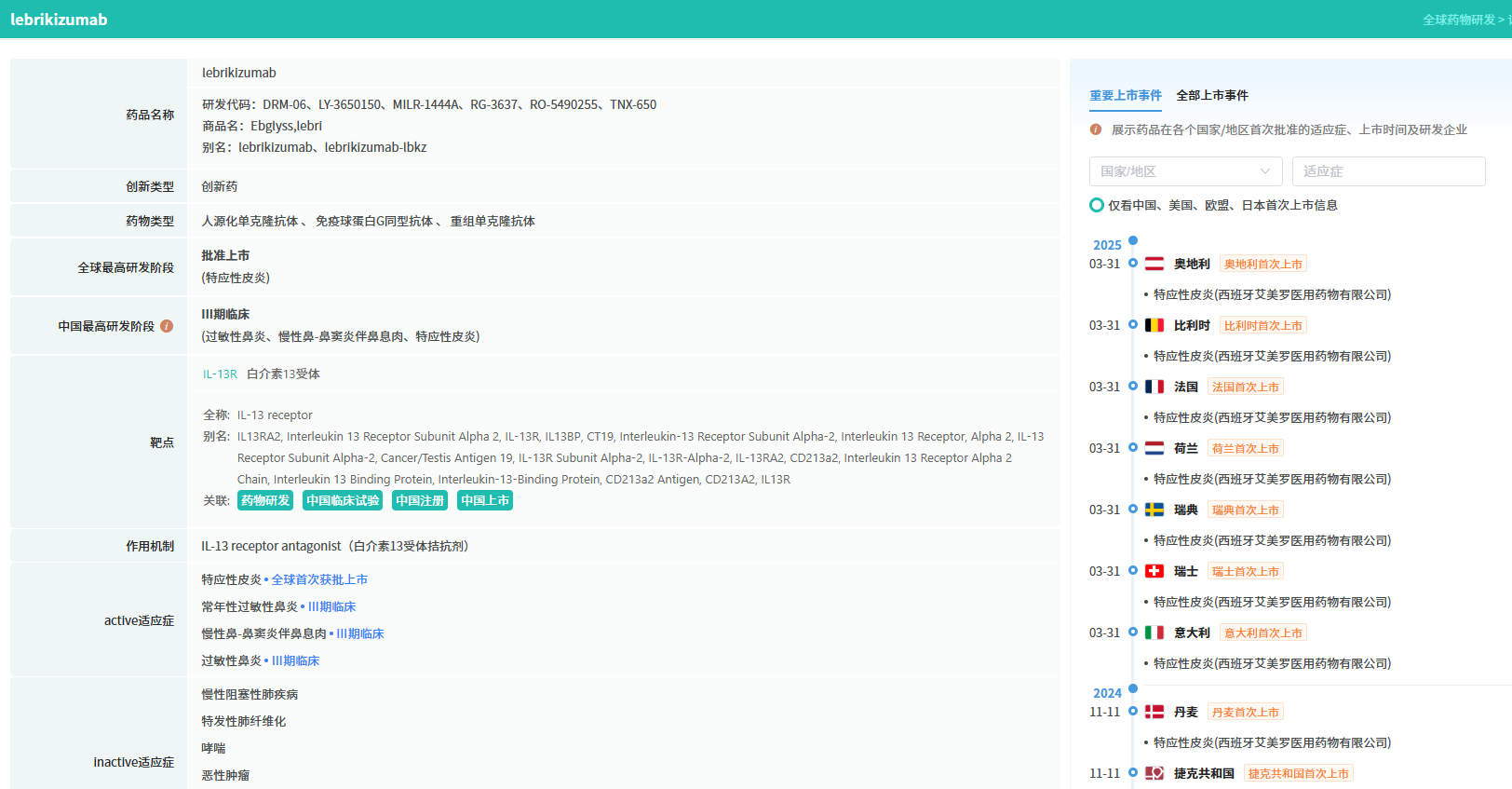
查数据,找摩熵!图源:全球药物研发数据库
与传统广谱免疫抑制剂不同,来瑞奇珠单抗 通过精准阻断IL-13信号通路,从源头抑制炎症反应,从而在减轻症状的同时,尽可能保留皮肤的正常生理功能。这一机制使其在疗效与安全性之间展现出较好的平衡潜力。
二、命运转折:从罗氏到礼来的十六年研发长跑
据礼来2025年报,来瑞奇珠单抗 在全球销售额约为4.08亿美元。这款药物的的开发历程堪称一波三折,其归属权的多次流转本身就是一部跨国药企的战略变迁史:
- 2008年:由罗氏原研启动首个临床试验,首发适应症锁定哮喘,但进展不顺;
- 2016年:在哮喘的两项III期临床中“一胜一败”,商业化前景蒙上阴影;
- 2017年8月:罗氏将该药授权转让给Dermira公司,转向皮肤病领域;
- 2019年:Dermira又将欧洲地区商业化选择权转让给Almirall,进一步分散风险;
- 2020年:礼来完成对Dermira的整体收购,正式将这一“遗珠”收入麾下。
在礼来的操盘下,来瑞奇珠单抗 的潜力被重新激活。2023年至2024年间,其先后获欧盟、日本及美国批准,用于治疗成人及12岁以上儿童中重度特应性皮炎患者,迅速跻身全球皮肤病治疗市场的“新贵”行列。
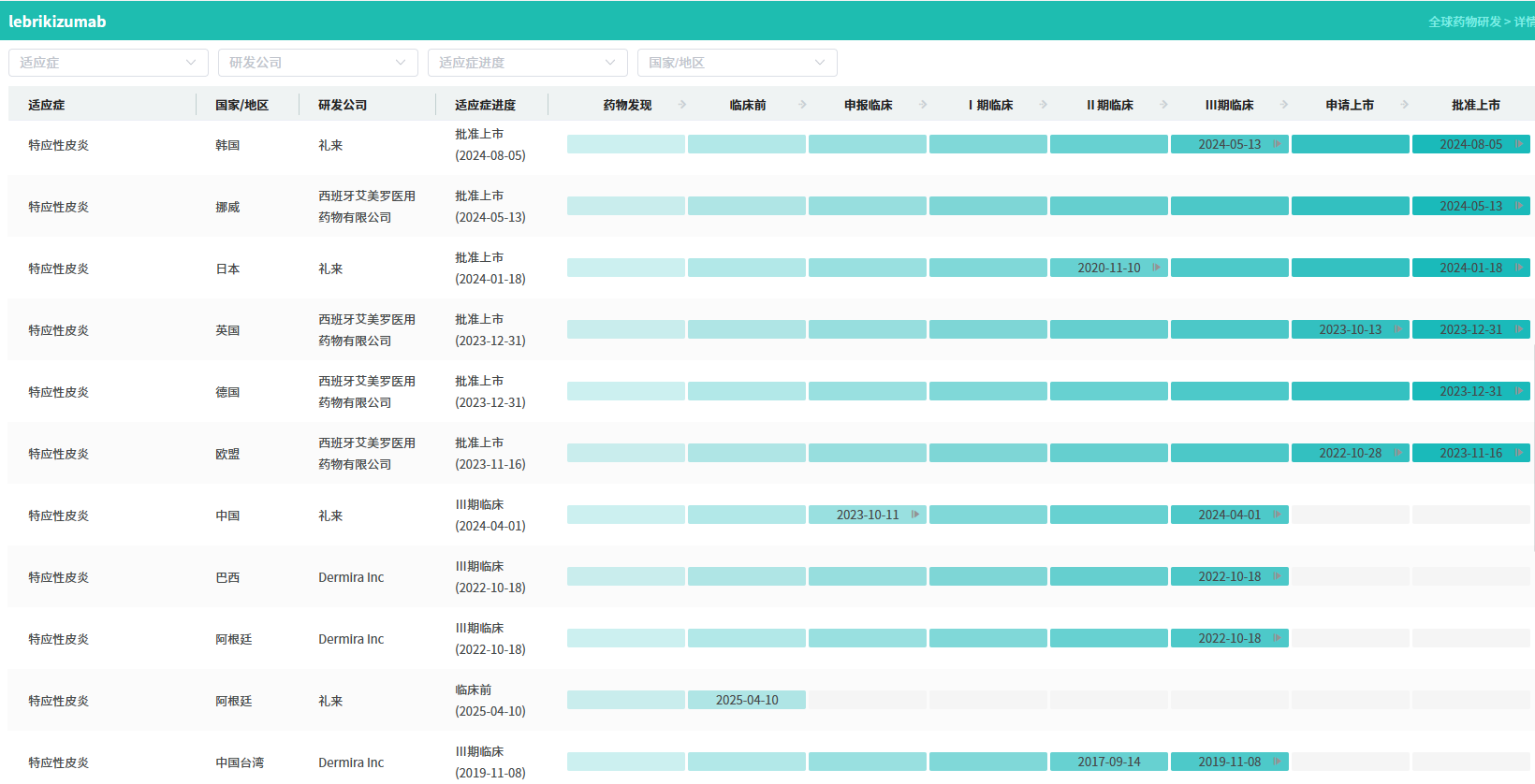
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
三、国内赛场:接力度普利尤,特应性皮炎治疗格局生变
目前,国内特应性皮炎生物制剂市场由赛诺菲的 度普利尤单抗(IL-4Rα抑制剂)一家独大。来瑞奇珠单抗 的IL-13靶点机制与之形成差异化互补,有望在疗效持久性、瘙痒控制等方面提供新的优势。据摩熵医药数据库显示,目前全球有2款IL-13单抗获批上市,涉及利奥制药的 Tralokinumab 和礼来的 来瑞奇珠单抗 。

查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
此次礼来在国内申报上市,不仅是其皮肤科管线的重要里程碑,也可能引发新一轮的市场竞争与用药格局重塑。随着审评进程的推进,国内患者有望在不远的将来,迎来第二款IL-13靶向疗法的选择。
参考来源:
[1] CDE官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 2025年全球药企TOP10洗牌:礼来登顶、默沙东跌出前五,GLP-1双雄对决,代谢领域彻底“翻身”
2. 礼来GLP-1R/GIPR双重激动剂「替尔泊肽」国内第5项适应症获批,全球版图与后续布局全解析
3. 礼来2025年财报全景:营收飙升,市值破万亿,基因疗法与核药临床管线终止
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论