
4月1日,礼来公司宣布,其口服小分子GLP-1受体激动剂Orforglipron(奥氟格列隆)已获得美国FDA批准上市,用于治疗成人肥胖或超重。这是全球首个获批上市的口服小分子非肽类GLP-1受体激动剂,标志着小分子口服减重药物正式进入临床应用时代。

截图来源:礼来企业官网
Orforglipron是一种每日一次的口服小分子GLP-1受体激动剂,最初由中外制药发现,2018年礼来获得其开发授权并推进后续临床研究。该药服用便捷,可在全天任意时间服用,且不受饮食、饮水限制,患者依从性预期较高。
一、基于ATTAIN系列研究,疗效与便利性并重
此次获批主要基于ATTAIN系列Ⅲ期临床研究的积极结果。该研究包含两项全球注册试验,共纳入超过4500例肥胖或超重患者。
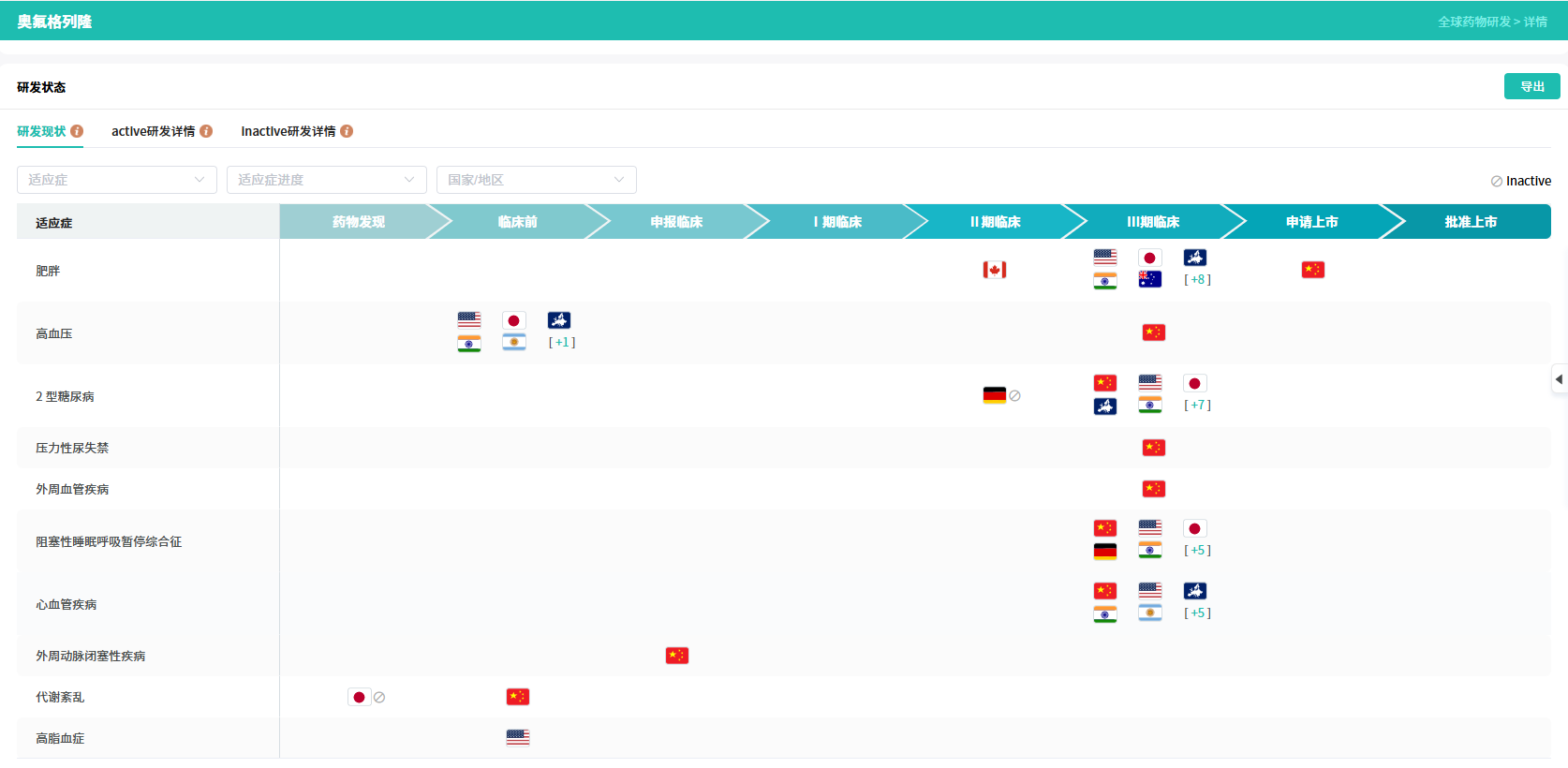
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
2025年8月,礼来公布了Orforglipron治疗肥胖的Ⅲ期临床ATTAIN-1研究的顶线数据:36mg高剂量组治疗72周实现减重11.5%(安慰剂校正后)。根据获批说明书,Orforglipron起始剂量为0.8mg,可在至少30天后增至2.5mg,再经至少30天调整至5.5mg,目标剂量分别为9mg、14.5mg、17.2mg,具体根据治疗反应和耐受性确定。
二、适应症持续拓展,中国布局同步推进
目前,礼来正在推进Orforglipron多项Ⅲ期研究,包括用于2型糖尿病、肥胖或超重伴有体重相关合并症患者的系列临床试验。此外,该药还在探索用于治疗肥胖成人合并阻塞性睡眠呼吸暂停、高血压及骨关节炎疼痛的潜在价值。
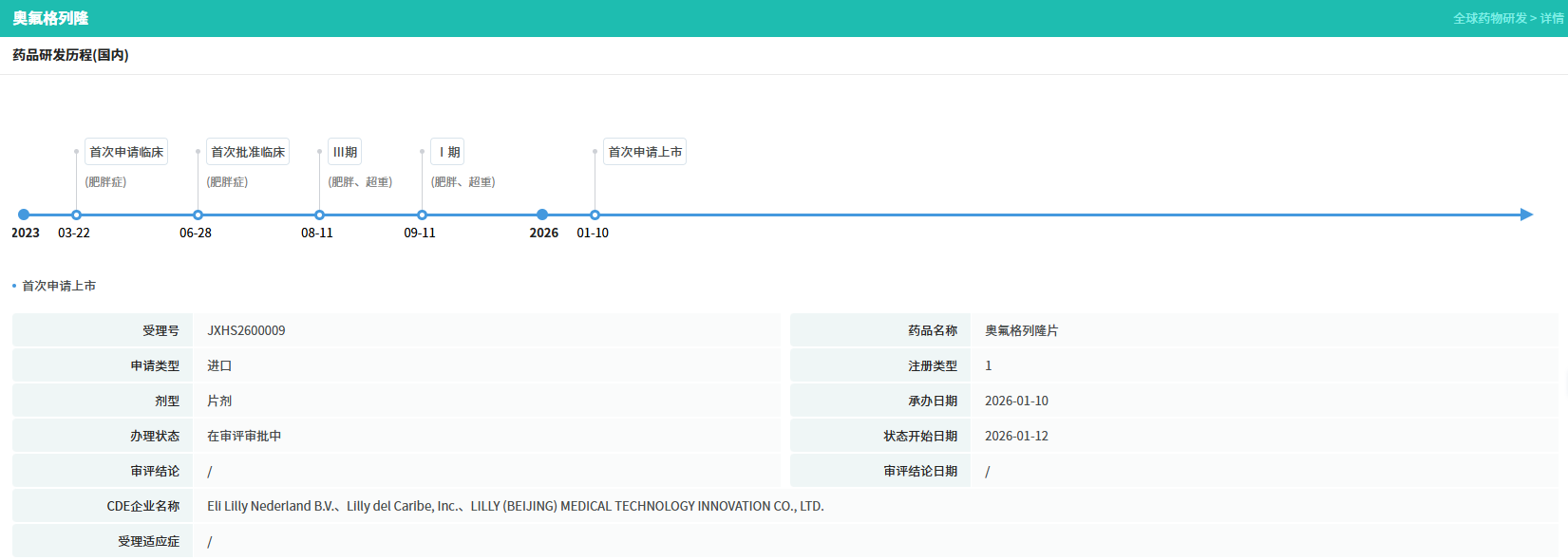
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
在中国,国家药监局药品审评中心已于2026年1月受理了奥氟格列隆片的上市申请,用于治疗2型糖尿病与肥胖症。今年3月11日,礼来宣布计划未来十年在中国累计投资30亿美元,全面扩展供应链产能,打造口服固体制剂本土生产与供应体系,其中Orforglipron的生产能力建设是重要布局方向。
三、口服减重药物市场加速形成,竞争持续升级
2025年底,诺和诺德口服司美格鲁肽获批用于减重,上市3周内即达到每周5万张处方,放量速度远超历史注射剂型,凸显市场对口服减重药物的旺盛需求。
礼来的Orforglipron作为首款小分子GLP-1口服药物,在生产成本、给药便利性上具备优势,虽然其减重疗效数据与部分注射剂型仍有一定差距,但其口服给药方式预计将显著提升患者长期用药意愿。
值得注意的是,礼来并未止步于Orforglipron。公司已通过合作引进英矽智能开发的下一代小分子GLP-1药物,该药物具备更好疗效、每周一次给药的潜力,显示出礼来在口服GLP-1赛道持续加码、迭代产品的战略布局。
四、结语
随着Orforglipron的获批,全球减重药物市场正式进入“口服时代”。在巨大临床需求与激烈研发竞争的双重驱动下,更多差异化、便利化的治疗方案有望加速涌现,为肥胖患者提供更丰富、可及的治疗选择。
参考来源:
[1] 企业官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 口服GLP-1双雄争霸:诺和诺德口服司美格鲁肽提交FDA,礼来orforglipron如何接招?
2. 礼来Orforglipron破局GLP-1:口服小分子引领新风尚,国产玩家蓄势待发
3. 礼来股价大跌6%!GLP-1药物收入未达预期,新药orforglipron或成希望
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论